reacciones de precipitación y reglas de solubilidad
una reacción de precipitación es aquella en la que las sustancias disueltas reaccionan para formar uno (o más) productos sólidos. Muchas reacciones de este tipo implican el intercambio de iones entre compuestos iónicos en solución acuosa y a veces se conocen como reacciones de doble desplazamiento, doble reemplazo o metátesis., Estas reacciones son comunes en la naturaleza y son responsables de la formación de arrecifes de coral en las aguas oceánicas y cálculos renales en los animales. Se utilizan ampliamente en la industria para la producción de una serie de productos básicos y productos químicos especializados. Las reacciones de precipitación también juegan un papel central en muchas técnicas de análisis químico, incluyendo pruebas puntuales utilizadas para identificar iones metálicos y métodos gravimétricos para determinar la composición de la materia (ver el último módulo de este capítulo).,
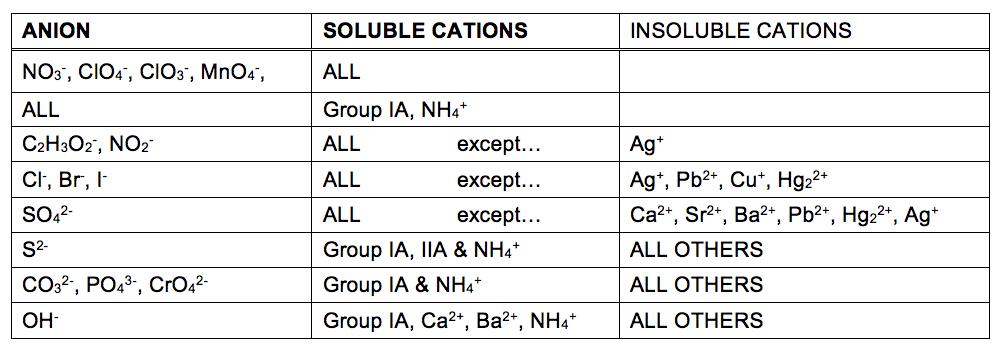
la medida en que una sustancia puede disolverse en agua o en cualquier disolvente se expresa cuantitativamente como su solubilidad, definida como la concentración máxima de una sustancia que puede alcanzarse en condiciones especificadas. Se dice que las sustancias con solubilidades relativamente grandes son solubles. Una sustancia se precipita cuando las condiciones de la solución son tales que su concentración excede su solubilidad. Se dice que las sustancias con solubilidades relativamente bajas son insolubles, y estas son las sustancias que precipitan fácilmente de la solución., Se proporciona más información sobre estos importantes conceptos en el capítulo del texto sobre soluciones. Para los propósitos de predecir las identidades de los sólidos formados por reacciones de precipitación, uno puede simplemente referirse a los patrones de solubilidad que se han observado para muchos compuestos iónicos (Tabla 1).
Un ejemplo vivo de precipitación se observa cuando se mezclan soluciones de yoduro de potasio y nitrato de plomo, lo que resulta en la formación de yoduro de plomo sólido:
esta observación es consistente con las pautas de solubilidad: el único compuesto insoluble entre todos los involucrados es el yoduro de plomo, una de las excepciones a la solubilidad general de las sales de yoduro.,
la ecuación iónica neta que representa esta reacción es:
. Las propiedades de los cristales puros de PbI2 los hacen útiles para la fabricación de detectores de rayos X y rayos gamma.

la tabla de solubilidad de la tabla 1 puede usarse para predecir si se producirá una reacción de precipitación cuando se mezclen soluciones de compuestos iónicos solubles. Uno simplemente necesita identificar todos los iones presentes en la solución y luego considerar si es posible el emparejamiento catión/anión podría resultar en un compuesto insoluble.
por ejemplo, mezclar soluciones de nitrato de plata y fluoruro de sodio producirá una solución que contiene iones Ag+, No3−, Na+ y f−., Aparte de los dos compuestos iónicos originalmente presentes en las soluciones, AgNO3 y NaF, dos compuestos iónicos adicionales pueden derivarse de esta colección de iones: NaNO3 y AgF.
la tabla de solubilidad indica que todas las sales de nitrato son solubles, pero que el AgF es una de las excepciones a la solubilidad general de las sales de fluoruro. Una reacción de precipitación, por lo tanto, se predice que ocurra, como se describe por las siguientes ecuaciones: