Learning Objectives
- describir una molécula de anticuerpo.
- dibuje la estructura de la» figura de palo » de IgG, indicando la porción Fab (región variable) y la porción Fc (región constante).
- indique las funciones de las porciones Fab y Fc de un anticuerpo.
- indique lo que se entiende por actividad biológica de un anticuerpo.
- Compare la estructura de IgM e Iga secretora con la de IgG.
en esta sección veremos la estructura de los anticuerpos., Existen cinco clases o isotipos de anticuerpos humanos:
- inmunoglobulina G (IgG),
- inmunoglobulina M (IgM),
- inmunoglobulina A (IgA),
- inmunoglobulina D (IgD), y
- inmunoglobulina E (IgE).
los anticuerpos más simples, como IgG, IgD e IgE, son macromoléculas en forma de «Y»llamadas monómeros. Un monómero se compone de cuatro cadenas de glicoproteína: dos cadenas pesadas idénticas y dos cadenas ligeras idénticas. Las dos cadenas pesadas tienen un alto peso molecular que varía con la clase de anticuerpo., Las cadenas ligeras vienen en dos variedades: kappa o lambda y tienen un peso molecular más bajo que las cadenas pesadas. Las cuatro cadenas de glicoproteínas están conectadas entre sí por enlaces disulfuro (S-S) y enlaces no covalentes (figura \(\PageIndex{1}\)).
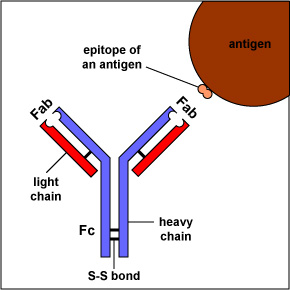
los enlaces S-S adicionales doblan las cadenas de glicoproteínas individuales en un número de dominios globulares distintos (figura \(\PageIndex{2}\)). El área donde la parte superior de la «Y» se une a la parte inferior se llama la bisagra. Esta área es flexible para permitir que el anticuerpo ate a pares de epítopos varias distancias aparte en un antígeno.
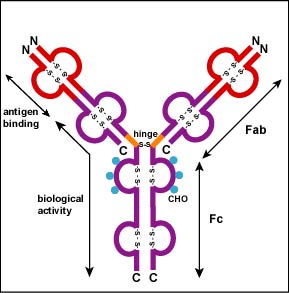
las dos puntas del monómero «y» se denominan fragmentos de unión al antígeno o porciones Fab del anticuerpo (Figuras 1-3)., Los primeros 110 aminoácidos o primer dominio de la cadena pesada y ligera de la región Fab del anticuerpo proporcionan especificidad para unir un epítopo a un antígeno. La secuencia de aminoácidos de este primer dominio tanto de la cadena ligera como de la cadena pesada muestra una tremenda variación de anticuerpo a anticuerpo y constituye la región variable (región V)., Esto se debe a que cada linfocito B, Al principio de su desarrollo, se programa genéticamente a través de una serie de reacciones de empalme genético para producir un Fab con una forma única de 3 dimensiones capaz de ajustar algún epítopo con una forma correspondiente.
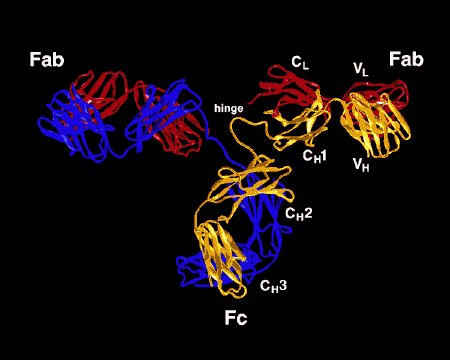
Figure \(\PageIndex{3}\): dibujo de cinta de la molécula de anticuerpo IgG2a, un dibujo de cinta de la primera molécula de anticuerpo intacta cristalizada (IgG2a). La porción Fab del anticuerpo tiene especificidad para atar un epítopo de un antígeno. La porción Fc dirige la actividad biológica del anticuerpo.,
Los diversos genes que las células empalman juntos determinan el orden de los aminoácidos de la porción Fab de la cadena ligera y pesada; la secuencia de aminoácidos determina la forma tridimensional final (figura \(\PageIndex{4}\)). Por lo tanto, diferentes moléculas de anticuerpos producidas por diferentes linfocitos B tendrán diferentes órdenes de aminoácidos en las puntas de la Fab para darles formas únicas para el epítopo de unión. El sitio de unión al antígeno es lo suficientemente grande como para contener un epítopo de aproximadamente 5-7 aminoácidos o 3-4 residuos de azúcar., Los epítopos se unen a la porción Fab del anticuerpo mediante enlaces reversibles no covalentes.
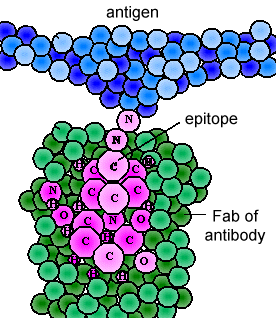
la parte inferior de la «y», la región cada cadena de glicoproteína, se llama la porción FC., La porción Fc, así como un dominio de la cadena pesada y ligera de la región Fab tiene una secuencia constante de aminoácidos y se conoce como la región constante (región C) del anticuerpo y define la clase y subclase de cada anticuerpo. La porción Fc es responsable de la actividad biológica del anticuerpo (Figuras 1-3), sin embargo, la porción Fc solo se vuelve biológicamente activa después de que el componente Fab se haya unido a su antígeno correspondiente., Dependiendo de la clase y subclase de anticuerpos, las actividades biológicas de la porción Fc de anticuerpos incluyen la capacidad de:
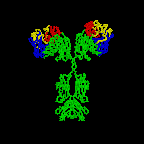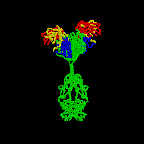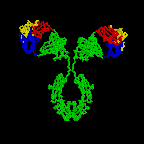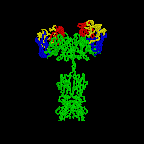
Las moléculas individuales de anticuerpos en forma de «y»se llaman monómeros y pueden unirse a dos epítopos idénticos. Los anticuerpos de las clases IgG, IgD e IgE son monómeros.
Dos clases de anticuerpos son más complejos., IgM (ver figura \(\PageIndex{10}\)) es un pentámero, que consiste en 5 moléculas similares a «Y»conectadas en sus porciones Fc por una «J» o cadena de unión. La IgA secretora (ver figura \(\PageIndex{11}\)) es un dímero que consiste en 2 moléculas similares a «Y»conectadas en sus porciones Fc por una cadena «J» y estabilizadas para resistir la digestión enzimática en las secreciones corporales por medio de un componente secretor.
resumen
- hay 5 clases o isotipos de anticuerpos humanos o inmunoglobulinas: IgG, IgM, IgA, IgD e IgE.,
- Los anticuerpos más simples, como IgG, IgD e IgE, son macromoléculas en forma de «Y»llamadas monómeros y se componen de cuatro cadenas de glicoproteína: dos cadenas pesadas idénticas y dos cadenas ligeras idénticas.
- Las dos puntas del monómero » Y » se conocen como los fragmentos de unión al antígeno o porciones Fab del anticuerpo y estas porciones proporcionan especificidad para unir un epítopo a un antígeno.,
- Al principio de su desarrollo, cada linfocito B se programa genéticamente a través de una serie de reacciones de empalme genético para producir un Fab con una forma única de 3 dimensiones capaz de encajar algún epítopo con una forma correspondiente.
- La porción Fc solo se vuelve biológicamente activa después de que el componente Fab se ha unido a su antígeno correspondiente. Las actividades biológicas incluyen la activación de las vías del complemento y la unión a los receptores de los fagocitos y otras células de defensa para promover la inmunidad adaptativa.
- IgM es un pentámero, que consiste en 5 monómeros Unidos en sus porciones Fc.,
- IgA es un dímero, que consiste en 2 monómeros Unidos en sus porciones Fc.
preguntas
estudie el material en esta sección y luego escriba las respuestas a estas preguntas. No haga clic en las respuestas y escríbalas. Esto no pondrá a prueba su comprensión de este tutorial.
- describir una molécula de anticuerpo. (ans)
- coincide con lo siguiente:
_____ la región del anticuerpo que proporciona especificidad para unir un epítopo a un antígeno., (ans)
_____ la región del anticuerpo que es responsable de la actividad biológica del anticuerpo. (ans)
_____ compuesto de cuatro cadenas de glicoproteínas. Hay dos cadenas pesadas idénticas que tienen un alto peso molecular y dos cadenas ligeras idénticas. (ans)
_____ pentámero, que consiste en 5 moléculas similares a «Y»conectadas en sus porciones Fc por una «J» o cadena de unión. (ans)
_____ un dímero que consiste en 2 moléculas similares a «Y»conectadas en sus porciones Fc por una cadena «J» y estabilizadas para resistir la digestión enzimática., (ans)
- IgM
- IgA secretora
- IgG
- Fab
- Fc
- Opción Múltiple (ans)
los Contribuyentes y Atribuciones
-
el Dr. Gary Kaiser (UNIVERSIDAD de COMUNIDAD del CONDADO DE BALTIMORE, CATONSVILLE CAMPUS)