12.7 buffere
læringsmål
- Definer buffer.
- Identificer korrekt de to komponenter i en buffer.
Som angivet i Afsnit 12.4 “Stærke og Svage Syrer og Baser og Deres Salte”, svage syrer er relativt almindelige, selv i de fødevarer, vi spiser. Men vi støder lejlighedsvis på en stærk syre eller base, såsom mavesyre, som har en stærkt sur pH på 1, 7. Per definition kan stærke syrer og baser producere en relativt stor mængde H+ eller OH− ioner og har følgelig markante kemiske aktiviteter., Derudover kan meget små mængder stærke syrer og baser ændre pH i en opløsning meget hurtigt. Hvis der blev tilsat 1 mL mavesyre til blodbanen, og der ikke var nogen korrektionsmekanisme, ville blodets pH falde fra omkring 7, 4 til omkring 4, 7-en pH, der ikke er befordrende for fortsat Levevis. Heldigvis har kroppen en mekanisme til at minimere sådanne dramatiske pH-ændringer.
mekanismen involverer en bufferA-løsning, der modstår dramatiske ændringer i pH., en løsning, der modstår dramatiske ændringer i pH., Buffere gør det ved at være sammensat af visse par opløste stoffer: enten en svag syre plus et salt afledt af den svage syre eller en svag base plus et salt af den svage base. For eksempel kan en buffer være sammensat af opløst HC2H3O2 (en svag syre) og NaC2H3O2 (saltet afledt af den svage syre). Et andet eksempel på en buffer er en opløsning indeholdende NH3 (en svag base) og NH4Cl (et salt afledt af den svage base).
lad os bruge en HC2H3O2 / NaC2H3O2 buffer til at demonstrere, hvordan buffere fungerer., Hvis en stærk base—en kilde af OH−(aq) ioner—er føjet til den buffer løsning, dem, OH− ioner vil reagere med HC2H3O2 i en syre-base reaktion:
HC2H3O2(aq) + OH−(aq) → H2O(g ar) + C2H3O2−(aq)
Stedet for at ændre pH dramatisk ved at gøre den løsning, der grundlæggende, den ekstra OH− ioner reagerer med at gøre H2O, så pH-værdien ændrer sig ikke meget.
Hvis der tilsættes en stærk syre—en kilde til H+—ioner-til bufferopløsningen, reagerer H+ – ionerne med anionen fra saltet. Fordi HC2H3O2 er en svag syre, er det ikke ioniseret meget., Dette betyder, at hvis der masser af H+ – ioner og C2H3O2− ioner er til stede i den samme løsning, og de vil komme sammen for at gøre HC2H3O2:
H+(aq) + C2H3O2−(aq) → HC2H3O2(aq)
Stedet for at ændre pH dramatisk, og det gør løsningen sure, den ekstra H+ ioner reagerer med at gøre molekyler af en svag syre. Figur 12.2 “the Actions of Buffers” illustrerer begge handlinger af en buffer.
Figur 12.2 Handlinger Buffere
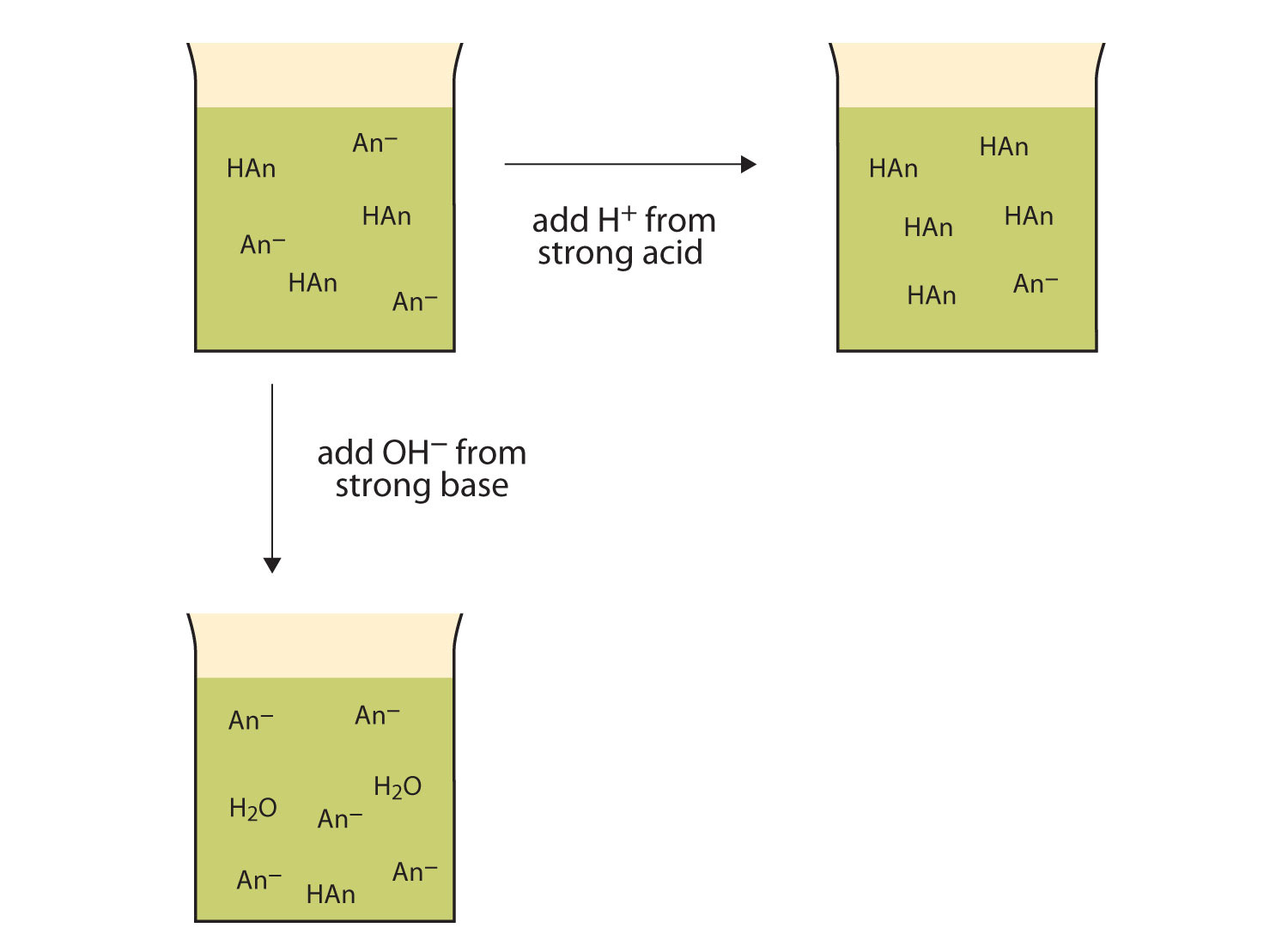
Buffere, der kan reagere med både stærke syrer (øverst) og stærke baser (side) for at minimere store ændringer i pH-værdien.,
buffere fremstillet af svage baser og salte af svage baser virker på samme måde. For eksempel, i en buffer, der indeholder NH3 og NH4Cl, NH3-molekyler, der kan reagere med nogen overskydende H+ – ioner, der er indført ved stærke syrer:
NH3(aq) + H+(aq) → NH4+(aq)
mens den NH4+(aq) ion kan reagere med nogen OH− ioner er indført med stærke baser:
NH4+(aq) + OH−(aq) → NH3(aq) + H2O(g ar)
Eksempel 15
Hvilke kombinationer af forbindelser, der kan gøre en buffer løsning?,
- HCHO2 og NaCHO2
- HCl og NaCl
- CH3NH2 og CH3NH3Cl
- NH3 og NaOH
Løsningen
- HCHO2 er myresyre, en svag syre, mens NaCHO2 er salt lavet af anion af den svage syre (den formate ion ). Kombinationen af disse to opløste stoffer ville gøre en bufferopløsning.
- HCl er en stærk syre, ikke en svag syre, så kombinationen af disse to opløste stoffer ville ikke lave en bufferopløsning.
- CH3NH2 er methylamin, som er som NH3 med et af dets H-atomer erstattet med en CH3-gruppe. Fordi det ikke er angivet i tabel 12.,2 “stærke syrer og baser”, kan vi antage, at det er en svag base. Forbindelsen CH3NH3Cl er et salt fremstillet af den svage base, så kombinationen af disse to opløste stoffer ville lave en bufferopløsning.
- NH3 er en svag base, men NaOH er en stærk base. Kombinationen af disse to opløste stoffer ville ikke gøre en bufferopløsning.
Test dig selv
hvilke kombinationer af forbindelser kan lave en bufferopløsning?,
- NaHCO3 og NaCl
- H3PO4 og NaH2PO4
- NH3 og NH4)3PO4
- NaOH og NaCl
Svar
- nej
- ja
- ja
- nej
Buffere arbejde godt kun i begrænsede mængder tilsat stærk syre eller base. Når enten opløst stof er fuldstændigt reageret, er opløsningen ikke længere en buffer, og der kan forekomme hurtige ændringer i pH. Vi siger, at en buffer har en vis kapacitetmængden af stærk syre eller base en buffer kan modvirke.., Buffere, der har mere opløst opløst i dem til at begynde med, har større kapacitet, som man kunne forvente.
humant blod har et buffersystem for at minimere ekstreme ændringer i pH. en buffer i blod er baseret på tilstedeværelsen af HCO3− og H2CO3 . Med denne buffer til stede, selvom nogle mavesyre skulle finde vej direkte ind i blodbanen, ville ændringen i blodets pH være minimal. Inde i mange af kroppens celler er der et bufferingssystem baseret på fosfationer.,
mad og drikke App: den syre, der letter smerter
selvom medicin ikke er nøjagtigt “mad og drikke”, indtager vi dem, så lad os se på en syre, der sandsynligvis er den mest almindelige medicin: acetylsalicylsyre, også kendt som aspirin. Aspirin er kendt som en smertestillende og antipyretisk (feber reducer).
strukturen af aspirin er vist i den ledsagende figur. Syredelen er cirkuleret; det er h-atomet i den del, der kan doneres, da aspirin virker som en Brønsted-lo .ry syre. Fordi det ikke er angivet i tabel 12.,2 “stærke syrer og baser”, acetylsalicylsyre er en svag syre. Det er dog stadig en syre, og i betragtning af at nogle mennesker forbruger relativt store mængder aspirin dagligt, kan dets sure natur forårsage problemer i maveforet, på trods af mavens forsvar mod sin egen mavesyre.12.3 den molekylære struktur af Aspirin
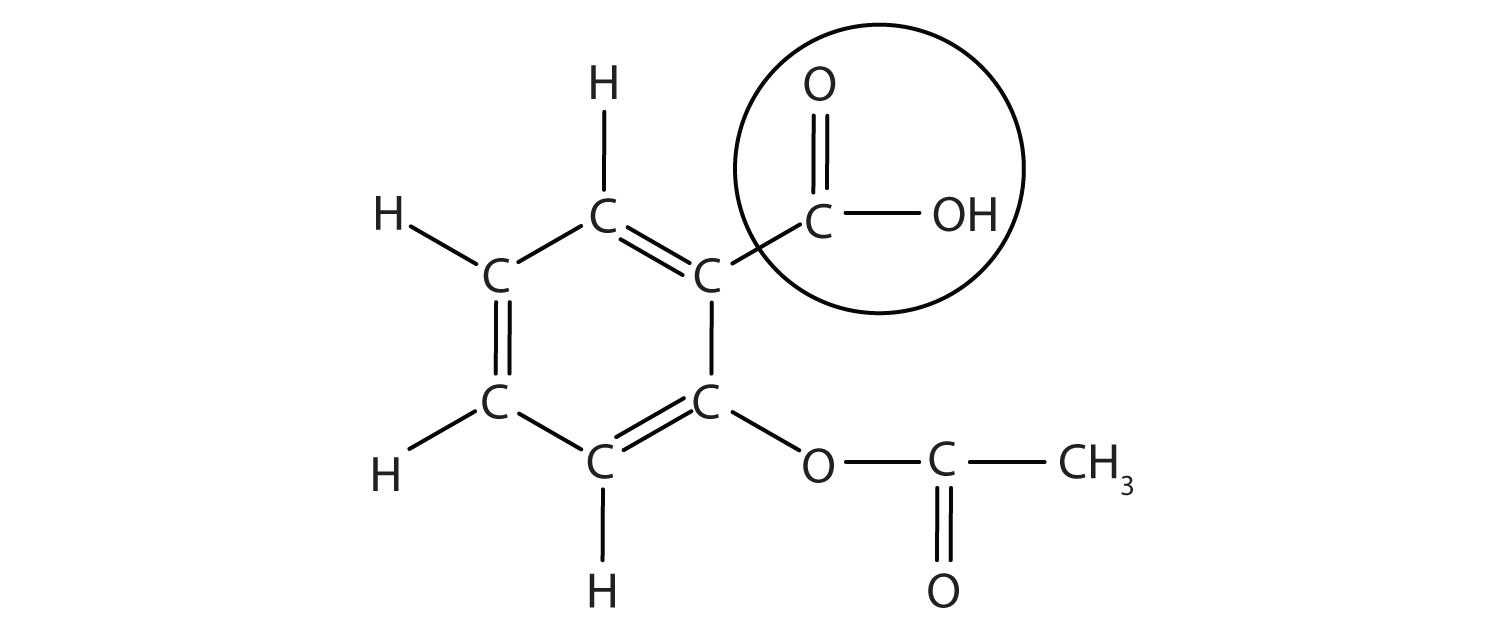
de cirklede atomer er den sure del af molekylet.
da aspirins syreegenskaber kan være problematiske, tilbyder mange aspirinmærker en “bufret aspirin” form af medicinen., I disse tilfælde indeholder aspirin også et buffermiddel—normalt MgO—der regulerer aspirinens surhed for at minimere dets sure bivirkninger.
så nyttigt og almindeligt som aspirin er, blev det formelt markedsført som et lægemiddel, der startede i 1899. US Food and Drug Administration (FDA), det statslige organ, der har til opgave at føre tilsyn med og godkende lægemidler i USA, blev ikke dannet før 1906., Nogle har hævdet, at hvis FDA havde været dannet før aspirin blev indført, aspirin kan aldrig have fået godkendelse på grund af dets potentiale for bivirkninger—gastrointestinal blødning, ringen for ørerne, Reyes syndrom (en leverlidelse), og nogle allergiske reaktioner. For nylig er aspirin imidlertid blevet udråbt for dens virkninger ved at mindske hjerteanfald og slagtilfælde, så det er sandsynligt, at aspirin er her for at blive.
– Tasten Takeaway
- en buffer er En løsning, der modstår pludselige ændringer i pH-værdien.
Øvelser
-
Angiv buffer., Hvilke to relaterede kemiske komponenter er nødvendige for at lave en buffer?
-
kan der laves en buffer ved at kombinere en stærk syre med en stærk base? Hvorfor eller hvorfor ikke?
-
hvilke kombinationer af forbindelser kan lave en buffer? Antag vandige opløsninger.
- HCl og NaCl
- HNO2 og NaNO2
- NH4NO3 og HNO3
- NH4NO3 og NH3
-
Hvilke kombinationer af forbindelser, der kan gøre en buffer? Antag vandige opløsninger.,
- H3PO4 og Na3PO4
- NaHCO3 og Na2CO3
- NaNO3 og Ca(NO3)2)
- nr hn3 og NH3
-
For hver kombination i Øvelse 3, der er en buffer, skriv den kemiske ligninger for de reaktioner, der af den buffer-komponenter, når en stærk syre og en stærk base er tilføjet.
-
for hver kombination i Øvelse 4, der er en buffer, skal du skrive de kemiske ligninger for reaktionerne fra bufferkomponenterne, når der tilsættes en stærk syre og en stærk base.,
-
Den komplette phosphatbuffer system er baseret på fire stoffer: (H3PO4), H2PO4−, HPO42− og PO43−. Hvilke forskellige bufferopløsninger kan der laves af disse stoffer?
-
forklar hvorfor NaBr ikke kan være en komponent i enten en sur eller en basisk buffer.
-
Der fremstilles to opløsninger, der indeholder de samme koncentrationer af opløste stoffer. Den ene opløsning består af H3PO4 og Na3PO4, mens den anden består af HCN og NaCN. Hvilken løsning skal have den større kapacitet som en buffer?,
-
Der fremstilles to opløsninger, der indeholder de samme koncentrationer af opløste stoffer. Den ene løsning består af NH3 og NH4NO3, mens den anden består af H2SO4 og Na2SO4. Hvilken løsning skal have den større kapacitet som en buffer?
Svar
-
En buffer er kombinationen af en svag syre eller base og et salt af, at svag syre eller base.,
-
-
- nej
- ja
- nej
- ja
-
-
3b: stærk syre: NO2− + H+ → HNO2; stærk base: HNO2 + OH− → NO2− + H2O; 3d: stærk base: NH4+ + OH− → NH3 + H2O; stærk syre: NH3 + H+ → NH4+
-
-
Buffere kan være lavet af tre kombinationer: (1) H3PO4 og H2PO4−, (2) H2PO4− og HPO42−, og (3) HPO42− og PO43−. (Teknisk set kan en buffer fremstilles af to komponenter.,)
-
-
phosphatbufferen skal have den større kapacitet.
-