12.7 vyrovnávací paměti
cíle učení
- definují vyrovnávací paměť.
- správně identifikujte dvě složky vyrovnávací paměti.
jak je uvedeno v bodě 12.4 „silné a slabé kyseliny a báze a jejich soli“, slabé kyseliny jsou relativně běžné i v potravinách, které jíme. Občas se však setkáváme se silnou kyselinou nebo bází, jako je žaludeční kyselina, která má silně kyselé pH 1,7. Podle definice mohou silné kyseliny a báze produkovat relativně velké množství h+ nebo Oh− iontů a následně mají výrazné chemické aktivity., Kromě toho velmi malé množství silných kyselin a zásad může velmi rychle změnit pH roztoku. Pokud 1 mL žaludeční kyseliny byly přidány do krevního oběhu, a ne oprava mechanismus byl přítomen, pH krve sníží z o 7.4 o 4.7—pH, který není příznivé pro pokračující život. Naštěstí má tělo mechanismus pro minimalizaci takových dramatických změn pH.
mechanismus zahrnuje vyrovnávací paměťroztok, který odolává dramatickým změnám pH., řešení, které odolává dramatickým změnám pH., Pufry tak činí tím, že se skládají z určitých párů rozpuštěných látek: buď slabá kyselina plus sůl odvozená z této slabé kyseliny, nebo slabá báze plus sůl této slabé báze. Například pufr může být složen z rozpuštěného HC2H3O2 (slabá kyselina) a NaC2H3O2 (sůl odvozená z této slabé kyseliny). Dalším příkladem pufru je roztok obsahující NH3 (slabá báze) a NH4Cl (sůl odvozená z této slabé báze).
použijeme vyrovnávací paměť HC2H3O2/NaC2H3O2, abychom ukázali, jak fungují vyrovnávací paměti., Pokud silná základna—zdroj OH−(aq) ionty—je přidán do roztoku pufru, ty, OH− iontů bude reagovat s HC2H3O2 v acidobazické reakce:
HC2H3O2(aq) + OH−(aq) → H2O(ℓ) + C2H3O2−(aq)
Spíše než změna pH výrazně tím, že řešení základní, přidány ionty OH− reagují na to, aby H2O, takže pH příliš nemění.
Pokud se do pufrového roztoku přidá silná kyselina—zdroj iontů H+, ionty H + budou reagovat s aniontem ze soli. Protože HC2H3O2 je slabá kyselina, není příliš ionizována., To znamená, že pokud jsou ve stejném roztoku přítomny spousty iontů H+ a iontů C2H3O2:
H+(aq) + C2H3O2− (aq) → HC2H3O2(aq)
spíše než dramaticky změnit pH a učinit roztok kyselým, přidané ionty H+ reagují na molekuly slabé kyseliny. Obrázek 12.2 „akce nárazníků“ ilustruje obě akce vyrovnávací paměti.
obrázek 12.2 akce nárazníků
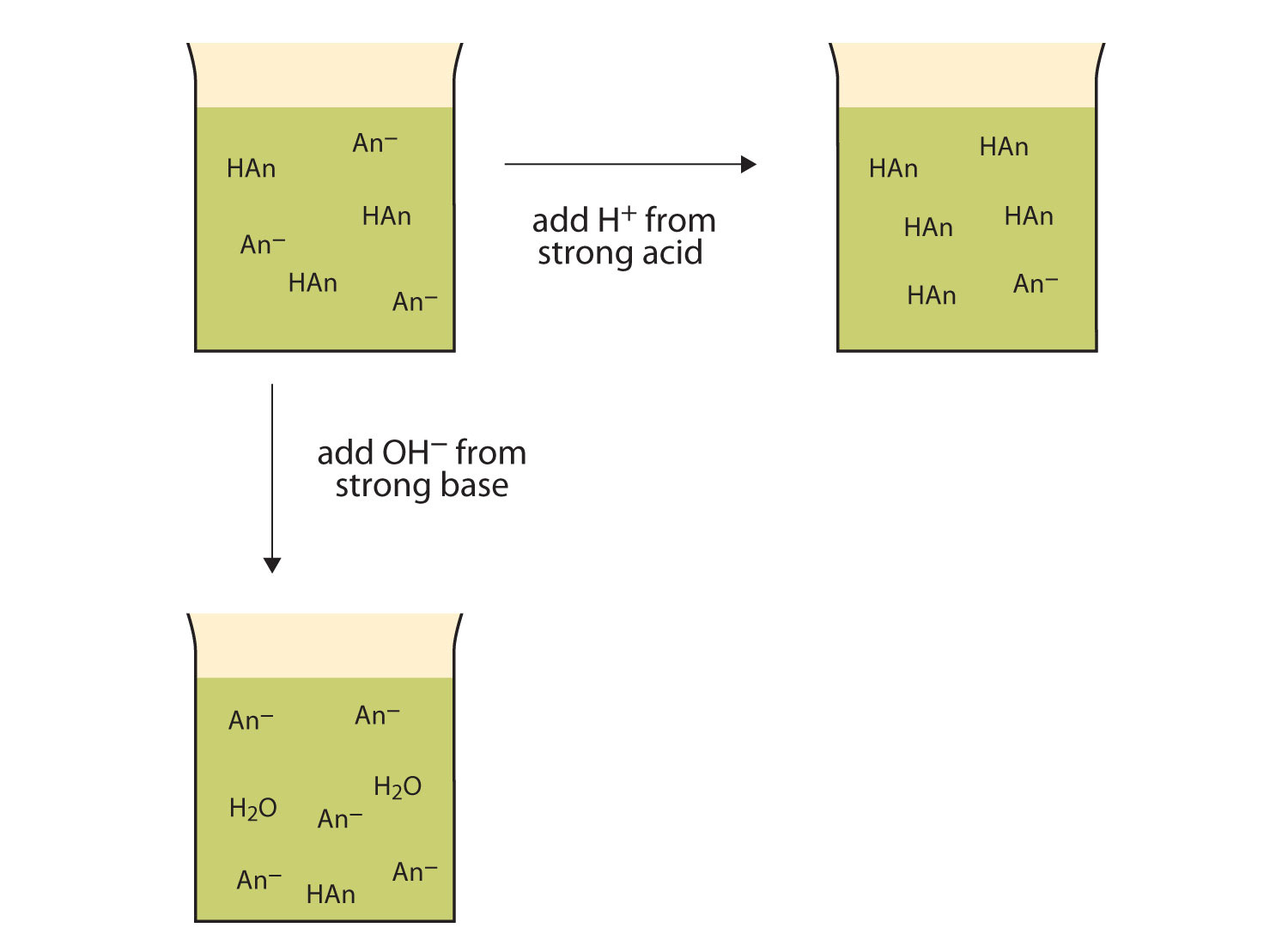
vyrovnávací paměti mohou reagovat jak se silnými kyselinami (nahoře), tak se silnými bázemi (stranou), aby se minimalizovaly velké změny pH.,
pufry vyrobené ze slabých bází a solí slabých bází působí podobně. Například, v pufru obsahující NH3 a NH4Cl, NH3 molekuly mohou reagovat s přebytečné H+ ionty zavedené silné kyseliny:
NH3(aq) + H+(aq) → NH4+(aq)
zatímco NH4+(aq) iont může reagovat s jakýmkoliv ionty OH− zavedená silná báze.
NH4+(aq) + OH−(aq) → NH3(aq) + H2O(ℓ)
Příklad 15
jaké kombinace sloučenin může mít tlumivý roztok?,
- HCHO2 a NaCHO2
- HCl a NaCl
- CH3NH2 a CH3NH3Cl
- NH3 a NaOH
Řešení
- HCHO2 je kyselina mravenčí, kyseliny, slabé kyseliny, zatímco NaCHO2 je sůl vyrobena z anion slabé kyseliny (formát ion ). Kombinace těchto dvou solutů by vytvořila vyrovnávací roztok.
- HCl je silná kyselina, ne slabá kyselina, takže kombinace těchto dvou solutů by nevytvářela pufrový roztok.
- CH3NH2 je methylamin, který je jako NH3 s jedním z jeho atomů H substituovaných skupinou CH3. Protože není uveden v tabulce 12.,2 „silné kyseliny a báze“, můžeme předpokládat, že se jedná o slabou základnu. Sloučenina CH3NH3Cl je sůl vyrobená z této slabé základny, takže kombinace těchto dvou solutů by vytvořila pufrový roztok.
- NH3 je slabá základna, ale NaOH je silná základna. Kombinace těchto dvou solutů by nevytvořila vyrovnávací roztok.
Otestujte se
které kombinace sloučenin mohou vytvořit pufrový roztok?,
- NaHCO3 a NaCl
- H3PO4 a NaH2PO4
- NH3 a (NH4)3PO4
- NaOH a NaCl
Odpovědi
- žádná
- ano
- ano
- žádná
Nárazníky fungují dobře pouze pro omezené množství přidané silné kyseliny nebo báze. Jakmile je buď rozpuštěná látka zcela reagována, roztok již není pufrem a může dojít k rychlým změnám pH. Říkáme, že pufr má určitou kapacitumnožství silné kyseliny nebo báze pufru může působit.., Nárazníky, které mají více rozpuštěné rozpuštěné látky, aby mohly začít, mají větší kapacity, jak by se dalo očekávat.
lidská krev má pufrační systém, který minimalizuje extrémní změny pH. jeden pufr v krvi je založen na přítomnosti HCO3− a H2CO3 . S tímto pufrem přítomným, i když by nějaká žaludeční kyselina našla cestu přímo do krevního řečiště, by změna pH krve byla minimální. Uvnitř mnoha buněk těla je pufrační systém založený na fosfátových iontech.,
Jídlo a Pití App: Kyselina, Která Zmírňuje Bolest
i když léky nejsou přesně „jídlo a pití“ my jsme jim potravu, takže pojďme se podívat na kyselinu, která je pravděpodobně nejčastější léky: kyselina acetylsalicylová, známý také jako aspirin. Aspirin je dobře známý jako lék proti bolesti a antipyretikum (redukce horečky).
struktura aspirinu je znázorněna na doprovodném obrázku. Kyselá část je zakroužkována; je to atom H v této části, který může být darován jako aspirin působí jako kyselina Brønsted-Lowry. Protože není uveden v tabulce 12.,2 „silné kyseliny a báze“, kyselina acetylsalicylová je slabá kyselina. Je to však stále kyselina a vzhledem k tomu, že někteří lidé denně konzumují relativně velké množství aspirinu, může jeho kyselá povaha způsobit problémy v žaludeční výstelce, a to navzdory obraně žaludku proti vlastní žaludeční kyselině.
Obrázek 12.3 Molekulární Struktura Aspirin
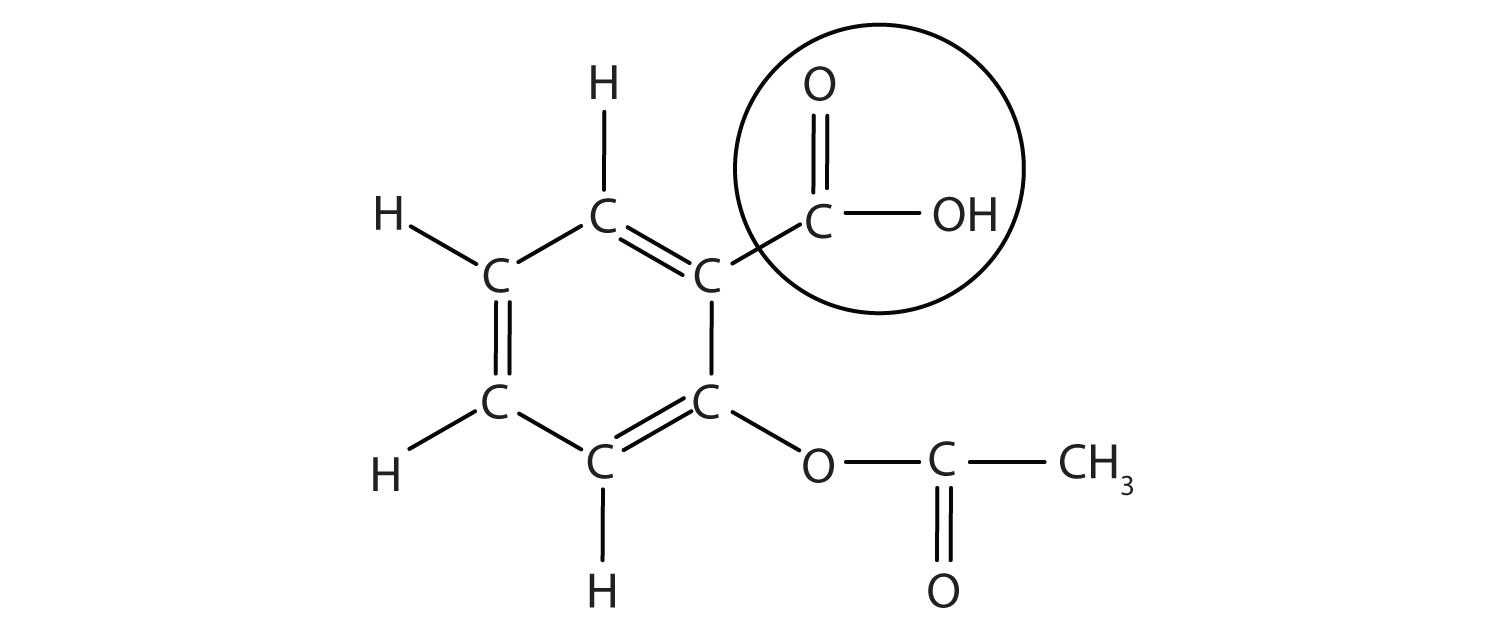
kroužil atomy jsou kyselina část molekuly.
protože kyselé vlastnosti aspirinu mohou být problematické, mnoho značek aspirinu nabízí formu léku „pufrovaný aspirin“., V těchto případech obsahuje aspirin také pufrační činidlo-obvykle MgO -, které reguluje kyselost aspirinu, aby se minimalizovaly jeho kyselé vedlejší účinky.
stejně užitečné a běžné jako aspirin, byl formálně uváděn na trh jako lék od roku 1899. Americká Food and Drug Administration (FDA), vládní agentura pověřená dohlížením a schvalováním drog ve Spojených státech, vznikla až v roce 1906., Někteří tvrdí, že pokud FDA byl vytvořen dříve, než aspirin byl představen, aspirin může nedostal schválení vzhledem k jeho potenciálu pro vedlejší účinky—gastrointestinální krvácení, zvonění v uších, Reyův syndrom (potíže s játry), a některé alergické reakce. Nedávno však byl aspirin nabízen pro jeho účinky při snižování srdečních záchvatů a mrtvice, takže je pravděpodobné, že aspirin zde zůstane.
Key Stánek s jídlem
- vyrovnávací paměť je řešení, které odolává náhlým změnám pH.
Cvičení
-
Definovat buffer., Jaké dvě související chemické složky jsou potřebné k vytvoření pufru?
-
může být pufr vytvořen kombinací silné kyseliny se silnou bází? Proč nebo proč ne?
-
které kombinace sloučenin mohou vytvořit pufr? Předpokládejme vodné roztoky.
- HCl a NaCl
- HNO2 a NaNO2
- NH4NO3 a HNO3
- NH4NO3 a NH3
-
jaké kombinace sloučenin může udělat rezervu? Předpokládejme vodné roztoky.,
- H3PO4 a Na3PO4
- NaHCO3 a Na2CO3
- NaNO3 a Ca(NO3)2
- HN3 a NH3
-
Pro každou kombinaci Cvičení 3, že je vyrovnávací paměť, napište chemické rovnice reakcí pufru komponenty, když to silná kyselina a silná báze, které je přidáno.
-
pro každou kombinaci ve cvičení 4, která je pufrem, napište chemické rovnice pro reakce složek pufru, když se přidá silná kyselina a silná báze.,
-
kompletní fosfátový pufrační systém je založen na čtyřech látek: H3PO4, H2PO4−, HPO42− a PO43−. Jaké různé pufrové roztoky mohou být vyrobeny z těchto látek?
-
vysvětlete, proč NaBr nemůže být složkou v kyselém nebo základním pufru.
-
jsou vyrobeny dva roztoky obsahující stejné koncentrace rozpuštěných látek. Jedno řešení se skládá z H3PO4 a na3po4, zatímco druhé se skládá z HCN a NaCN. Které řešení by mělo mít větší kapacitu jako vyrovnávací paměť?,
-
jsou vyrobeny dva roztoky obsahující stejné koncentrace rozpuštěných látek. Jedno řešení se skládá z NH3 a NH4NO3, zatímco druhé se skládá z H2SO4 a Na2SO4. Které řešení by mělo mít větší kapacitu jako vyrovnávací paměť?
Odpovědi
-
vyrovnávací paměť je směs slabé kyseliny nebo báze a soli této slabé kyseliny nebo báze.,
-
-
- žádná
- ano
- žádná
- ano
-
-
3b: silná kyselina: NO2− + H+ → HNO2; silná základna: HNO2 + OH− → NO2− + H2O; 3d: silná základna: NH4+ + OH− → NH3 + H2O; silná kyselina: NH3 + H+ → NH4+
-
-
Vyrovnávací paměti mohou být vyrobeny ze tří kombinací: (1) H3PO4 a H2PO4−, (2) H2PO4− a HPO42−, a (3) HPO42− a PO43−. (Technicky lze nárazník vyrobit z libovolných dvou komponent.,)
-
-
fosfátový pufr by měl mít větší kapacitu.
-