účelem lymfoidních orgánů je poskytnout tělu imunitu. Tento druhý článek v šestidílné sérii vysvětluje primární a sekundární lymfatické orgány a jejich klinický význam a strukturu. Je dodáván s self-assessment, která vám umožní vyzkoušet své znalosti po přečtení
Abstrakt
Tento článek je druhý ze šesti částí série o lymfatický systém. Diskutuje o roli lymfoidních orgánů, které mají rozvíjet a poskytovat imunitu tělu., Primárními lymfoidními orgány jsou červená kostní dřeň, ve které se produkují krevní a imunitní buňky, a brzlík, kde dozrávají T-lymfocyty. Lymfatické uzliny a slezina jsou hlavními sekundárními lymfoidními orgány; odfiltrují patogeny a udržují populaci zralých lymfocytů.
citace: Nigam Y, Knight J (2020) lymfatický systém 2: Struktura a funkce lymfatických orgánů. Ošetřovatelské Časy ; 116: 11, 44-48.,
autoři: Yamni Nigam je profesorem biomedicínské vědy; John Knight je docentem v biomedicínské vědě; oba na College of Human and Health Sciences, Swansea University.,
- Tento článek byl double-blind peer přezkoumány
- Přejděte dolů, abyste si přečíst článek, nebo stáhnout a vytisknout ve formátu PDF zde (v případě, že PDF nedokáže plně stáhnout, zkuste to prosím znovu pomocí jiného prohlížeče)
- Klikněte zde pro zobrazení dalších článků v této sérii
- Zhodnotit své znalosti a získat CPD důkazy tím, že Kojící Krát Self-assessment test
Úvod
Tento článek popisuje hlavní lymfatické orgány a jejich úlohy ve vývoji a poskytování imunity pro tělo., Lymfoidní orgány zahrnují červenou kostní dřeň, brzlík, slezinu a shluky lymfatických uzlin (obr. 1). Mají mnoho funkčních rolí v těle, zejména:
- Produkce krevních buněk, včetně červených krvinek (erytrocytů), bílých krvinek (leukocytů) a krevních destiček (trombocytů);
- Odstranění poškozených červených krvinek;
- Zrání imunitních buněk;
- Odchyt cizí materiál.,
červená kostní dřeň a brzlík jsou považovány za primární lymfatické orgány, protože v nich pochází většina imunitních buněk.

červené kostní dřeni
Kostní dřeň je měkká, rosolovitá tkáň v centrální dutině dlouhých kostí, jako jsou stehenní a pažní kosti. Krevní buňky a imunitní buňky vznikají z kostní dřeně; vyvíjejí se z nezralých kmenových buněk (hemocytoblastů), které sledují odlišné vývojové cesty, aby se staly buď erytrocyty, leukocyty nebo krevní destičky., Kmenové buňky se rychle množí, aby se miliardy krvinek každý den; tento proces je známý jako hematopoezy a je uvedena na Obr 2.

Pro zajištění nepřetržité výroby a diferenciace krevních buněk nahradit ty ztracené funkce nebo věku, hematopoetické kmenové buňky jsou přítomny v dospělosti. V embrya, krevní buňky jsou původně vyrobeny v žloutkového váčku, ale jako vývoj embrya probíhá, tato funkce je převzata sleziny, lymfatických uzlin a jater., Později v těhotenství převezme kostní dřeň většinu hematopoetických funkcí, takže při narození je celá kostra naplněna červenou kostní dření.
červená kostní dřeň produkuje všechny erytrocyty, leukocyty a krevní destičky. Hematopoetické kmenové buňky v kostní dřeni následovat buď myeloidní nebo lymfoidní linie vytvořit různé krevní buňky (Obr 2); patří mezi ně myeloidní progenitorové buňky (monocyty, makrofágy, neutrofily, bazofily, eozinofily, erytrocyty, dendritických buněk a krevních destiček), a lymfoidní progenitorové buňky (T-lymfocyty, B-lymfocyty a nk buňky).,
Některé lymfoidních buněk (lymfocytů), začít život v červené kostní dřeně a stát se plně vytvořeny v lymfatických orgánech, včetně brzlíku, sleziny a lymfatických uzlin. S dosažením puberty a zpomalením růstu dochází k fyziologické přeměně, která mění červenou kostní dřeň na žlutou kostní dřeň. Celý tento proces je dokončen ve věku 25 let, kdy distribuce červené kostní dřeně ukazuje svůj dospělý vzor v kostech.,
model je charakterizován:
- přítomnost červené kostní dřeně v axiálním skeletu (obratlů, křížové kosti a mediální části kyčelní kosti) a kloubní konce pažní a stehenní kosti;
- nejvíce distální části skeletu je naplněn žlutou kostní dřeň, která hlavně působí jako obchod pro tuky, poskytuje výživu a udržení správného prostředí pro kostní funkce.,
za zvláštních podmínek, jako je těžká ztráta krve nebo horečka, se však žlutá dřeň může vrátit zpět do červené dřeně (Malkiewicz a Dziedzic 2012).
onemocnění Kostní dřeně a transplantace
každá nemoc nebo porucha, která představuje hrozbu pro kostní dřeň může mít vliv na mnoho tělesných systémů, zvláště pokud brání kmenové buňky z stává základní buňky. Ty známo, že poškození dřeně je produktivní schopnosti a zničit kmenové buňky patří:
- Leukémie;
- Hodgkinova lymfomu;
- Další lymfomů.,
rostoucí počet onemocnění může být léčeni transplantací kostní dřeně nebo hematopoetických kmenových buněk, přenos; to je často dosaženo tím, že sklizeň vhodného dárce kmenových buněk z zadní kyčelní hřebeny kyčelní kosti, kde je koncentrace červené kostní dřeně je nejvyšší.
brzlík
brzlíku je bi-laločnaté, růžovo-šedá orgán se nachází těsně nad srdcem v mezihrudí, kde se odpočívá pod hrudní kostí (sternum)., Strukturálně se brzlík podobá malému motýlku, který postupně atrofuje (zmenšuje) s věkem. U pre-pubescentů je brzlík relativně velký a velmi aktivní orgán, který obvykle váží kolem 40 g, ale u dospělého středního věku se může dostatečně zmenšit, aby bylo obtížné ho najít., O 20 let věku, brzlík je o 50% menší, než tomu bylo při narození a ve věku 60 let se snížil na šestinu původní velikosti (Bilder, 2016); to se nazývá involuce brzlíku
Každý ze dvou laloků thymu je obklopen kapsle, ve které jsou četné malé lalůčky – typicky měření 2-3mm na šířku – které jsou drženy pohromadě pomocí volné pojivové tkáně., Každý lalůček se skládá z folikulů, které jsou složeny z rámce thyomsin žláz epiteliálních buněk a populací T-lymfocytů; tyto buňky jsou běžně označovány jako T-buňky („T“ značí jejich původu, jako zralé buňky z brzlíku). Lalůčky mají dvě odlišné oblasti:
- hustá vnější kůra, která je bohatá na aktivně dělení T-buněk;
- vnitřní dřeň, která je mnohem světlejší barvy a funkce, jako oblast T-buněčného zrání.,
kromě toho, že hlavní lymfoidní orgán, brzlíku je také uznána jako součást endokrinního systému, protože to vylučuje rodina hormonů souhrnně označovány jako thymosin; to je skupina několika strukturně příbuzných hormonů vylučovaných thymu epiteliální buňky. Tyto hormony jsou nezbytné pro normální imunitní funkce a mnoho členů thymosin rodině se používá terapeuticky k léčbě rakoviny, infekce a nemoci, jako je roztroušená skleróza (Severa et al, 2019).,
Role v zrání T-buněk
t-buňky vznikají jako hematopoetické kmenové buňky z červené kostní dřeně (obr. 2). Populace těchto hematopoetické kmenové buňky infiltrovat brzlík, dělících se dále do kortikálních oblastech lobules pak migrují do medulární regionů zrát do aktivních T-buněk; tento proces z T-buněk zrání je řízen hormon thymosin., Podíl těchto zralých T-buněk, neustále migrují z thymu do krve a dalších lymfoidních orgánů (slezina a lymfatické uzliny), kde hrají hlavní role v těle je specifické imunitní odpovědi (které budou podrobně popsány v části 3 této série). Význam těchto buněk je patrný u pacientů, kteří vyčerpali populace T-buněk, jako jsou pacienti infikovaní HIV.
Jednou z nejdůležitějších funkcí thymu je programování T-buňky rozpoznat “ já “ antigeny prostřednictvím procesu nazývaného thymu vzdělávání., Tento proces umožňuje zralým T-buňkám rozlišit cizí, a proto potenciálně patogenní materiál od antigenů, které patří do těla. Bylo prokázáno, že odstranění brzlíku může vést ke zvýšení autoimunitních onemocnění, jako je tato schopnost uznat vlastní je snížena (Sherer et al, 1999).
klinický význam
nemoci brzlíku zahrnují rakovinu brzlíku a myasthenia gravis (MG). MG nastává, když brzlík produkuje protilátky, které blokují nebo ničí místa svalových receptorů, což způsobuje, že svaly jsou slabé a snadno unavené., Nejčastěji postihuje svaly, které ovládají oči a oční víčka, což má za následek zvadlé oční víčka a potíže s výrazy obličeje; žvýkání, polykání a mluvení se také stávají obtížnými. MG může postihnout lidi v jakémkoli věku, ale obvykle začíná u žen ve věku <40 let a mužů ve věku >60 let.
ve většině případů MG nebo thymického karcinomu se doporučuje thymektomie., Pacienti, kteří měli tymektomie se může vyvinout selhání imunity známé jako Dobré syndrom, což zvyšuje jejich náchylnost k bakteriální, plísňové a virové oportunní patogeny; tato podmínka je však poměrně vzácné.
sleziny
sleziny a lymfatických uzlin jsou dvě hlavní sekundární lymfatické orgány, které hrají klíčovou roli v:
- Filtrování a ničí nežádoucí patogeny;
- Zachování populace zralých lymfocytů (což jsou bílé krvinky) umožní adaptivní imunitní odpověď na begin.,
když cizí antigeny dosáhnou těchto orgánů, iniciují aktivaci lymfocytů a následnou klonální expanzi a zrání těchto důležitých bílých krvinek. Zralé lymfocyty pak mohou opustit sekundární orgánů vstoupit do oběhu, nebo cestovat do jiných oblastí, a cílové cizí antigeny.
slezina je největší lymfoidní orgán., Nachází se v levé horní hypochondr oblasti břišní dutiny mezi membránou a fundu žaludku, je to v první řadě funguje jako filtr pro krev, přinášet to do blízkého kontaktu s úklid fagocyty (bílé krvinky ve slezině, která bude hledat a „jíst“ všechny patogeny v krvi) a lymfocyty.
díky rozsáhlé vaskularizaci je slezina tmavě purpurově oválným orgánem; u dospělých je přibližně 12 cm dlouhá, 7 cm široká a váží kolem 150 g., Nicméně, velikost sleziny se může lišit s okolnost: to snižuje při hladovění, po těžkém cvičení a následující závažné krvácení (Gujar et al, 2017), a poslední výzkumy ukazují nárůst velikosti v dobře živených jedinců a při požití potravin (Garnitschnig et al, 2020).
slezina (obr. 3) je uzavřena v husté, fibroelastické kapsli, která vyčnívá do orgánu jako trabekuly; tyto trabekuly tvoří rámec orgánu., Krev vstupuje do sleziny ze slezinné tepny a odchází přes slezinnou žílu, obě jsou v hilum; slezinná žíla se nakonec stává přítokem jaterní portální žíly.

slezina se skládá ze dvou regionů:
- Stroma rohovky – tvoří husté vnějšího pouzdra s jeho trabekuly, některé vláken a fibroblastů (buňky, které vylučují pojivové tkáně, kolagen);
- Parenchymu – skládá se ze dvou typů prolínání tkáně zvané bílé dužiny a červeným buničiny.,
Bílá dužnina je množství zárodečných center dělení B-lymfocyty (B-buňky), obklopen T-buněk a příslušenství buněk, včetně makrofágů a dendritických buněk; tyto buňky jsou uspořádány jako lymfatické uzliny kolem větve sleziny tepny. Jak krev proudí do sleziny přes slezinnou tepnu, vstupuje do menších centrálních tepen bílé buničiny a nakonec dosáhne červené buničiny. Červená dřeň je houbovitá tkáň, což představuje 75% objemu sleziny (Pivkin et al., 2016); skládá se z plné krve žilní dutin a sleziny šňůry.,
Sleziny šňůry jsou vyrobeny z červené a bílé krvinky a plazmatické buňky (protilátky produkují B-buňky); proto červené buničiny primárně funguje jako filtrační systém pro krev, vzhledem k tomu, že bílá dužnina je místo, kde adaptivní T – a B-buněčné odpovědi jsou namontovány. Barva bílé buničiny je odvozena od těsně zabalených lymfocytů a barva červené buničiny je způsobena vysokým počtem erytrocytů (Stewart and McKenzie, 2002).,
Funkce
slezina má tři hlavní funkce:
- Pro montáž imunitní reakce a odstranění mikroorganismů z oběhu;
- zničit poškozené a opotřebované červené krvinky;
- Pro uložení destiček (a krev).
hlavní imunologickou funkcí sleziny je odstranění mikroorganismů z oběhu. Lymfatické uzliny jsou uspořádány jako rukávy kolem krevních cév a přinášejí krev do sleziny., V bílé pulpě sleziny jsou uzlíky zvané Malpighian krvinky, které jsou bohaté na B-buňky, takže tato část lymfatické tkáně je rychle reagovat na cizí antigenní stimulace tím, že produkuje protilátky. Stěny meshwork sinusů v červené buničině také obsahují fagocyty, které pohlcují cizí částice a buněčné nečistoty, účinně je filtrují a odstraňují z oběhu.
při destrukci sleziny starých a senescentních červených krvinek jsou tráveny fagocytárními makrofágy v červené buničině. Poté se rozdělí na haem a globin., Globin je rozdělen na jednotlivé aminokyseliny, které lze využít při syntéze nového proteinu. Haem se skládá z atomu železa obklopeného čtyřmi neželeznými (pyrrolovými) kroužky.
železo je odstraněn a převezen být uloženy jako feritinu, pak znovu provést nové hemoglobinu v červené kostní dřeni; makrofágy převést pyrrolových kroužky do zeleného barviva biliverdin a pak se do žlutého pigmentu bilirubinu. Oba jsou transportovány do jater vázaných na plazmatický albumin., Bilirubin, toxičtější pigment, je konjugován v játrech za vzniku méně toxické sloučeniny, která se vylučuje žlučí.
červená buničina částečně slouží k uložení velké rezervy krevních destiček těla-až třetiny celkového přívodu krevních destiček. U některých zvířat – zejména sportovní savci, jako jsou koně, chrti a lišky – slezina je také významnou zásobárnou krve, která je uvolněna do oběhu v období stresu ke zlepšení aerobní výkonnosti., U lidí však slezina přispívá pouze malým procentem krevních buněk do aktivního oběhu za fyziologického stresu; celkový uložený objem krve je považován za pouze 200-250ml (Bakovic et al, 2005). Tobolka sleziny se může po krvácení snížit a uvolnit tuto rezervu do oběhu v těle.
slezina také hraje malou roli v hematopoezy: obvykle vyskytující se u plodů až pěti měsíců těhotenství, erytrocyty, spolu s kostní dřeni, jsou vyráběny sleziny.,
Klinický význam
Jako slezina je největší sbírka lymfatické tkáně v těle, infekce, které způsobují bílé krvinky proliferace a antigenní stimulace může způsobit germinálních center v orgánu rozšířit, což vede k jeho rozšíření (splenomegalie). To se děje u mnoha nemocí-například malárie, cirhózy a leukémie. Slezina není obvykle hmatatelná, ale zvětšená slezina je hmatatelná během hluboké inspirace. Zvětšení může být také způsobeno jakoukoli obstrukcí průtoku krve, například v jaterní portální žíle.,
odstranění
anatomická poloha sleziny se shoduje s levým desátým žebrem. Vzhledem ke své blízkosti k břišní stěně, je to jeden z nejčastěji poraněných orgánů u tupého poranění břicha. Slezina je křehký orgán a vzhledem ke své vysoce vaskularizované povaze jakékoli zranění způsobující prasknutí rychle povede k těžkému intraperitoneálnímu krvácení; smrt může vést k masivní ztrátě krve a šoku.
mírné zranění sleziny mohou být řešeny konzervativně, ale značně roztržení nebo protržení sleziny může být léčena kompletní a rychlé odstranění (splenektomie)., Současná data však podporují úspěšné neoperační řízení mnoha traumatických poranění sleziny se záměrem snížit potřebu úplného odstranění (Armstrong et al, 2019).
Pacienti léčeni pro některé maligní onemocnění může také vyžadovat částečné nebo úplné splenektomii a i jiné struktury, jako jsou kostní dřeně a jater může převzít některé funkce, které jsou obvykle prováděny ve slezině, u těchto pacientů může být zvýšené riziko infekce., S drtivou post-splenektomie infekce, tam je také zvýšené riziko sepse, která je spojena s významnou morbiditou a mortalitou. Infekce je obvykle zapouzdřenými patogeny, včetně Streptococcus pneumoniae, Haemophilus influenzae a Neisseria meningitidis. Klinické pokyny, které pomáhají snížit riziko infekce, obhajují vzdělávání o prevenci infekcí, očkování a profylaxi antibiotik (Arnott et al, 2018).,
„Otoky lymfatických uzlin a horečka jsou jistá znamení, že tělo je montáž efektivní imunitní odpovědi proti obtěžování patogen“
Lymfatických uzlin
Lymfatické uzliny se liší ve velikosti a tvaru, ale jsou obvykle ve tvaru fazole struktur klastru na konkrétních místech po celém těle. Ačkoli se jejich velikost liší, každý uzel má charakteristickou vnitřní strukturu (obr. 4).,
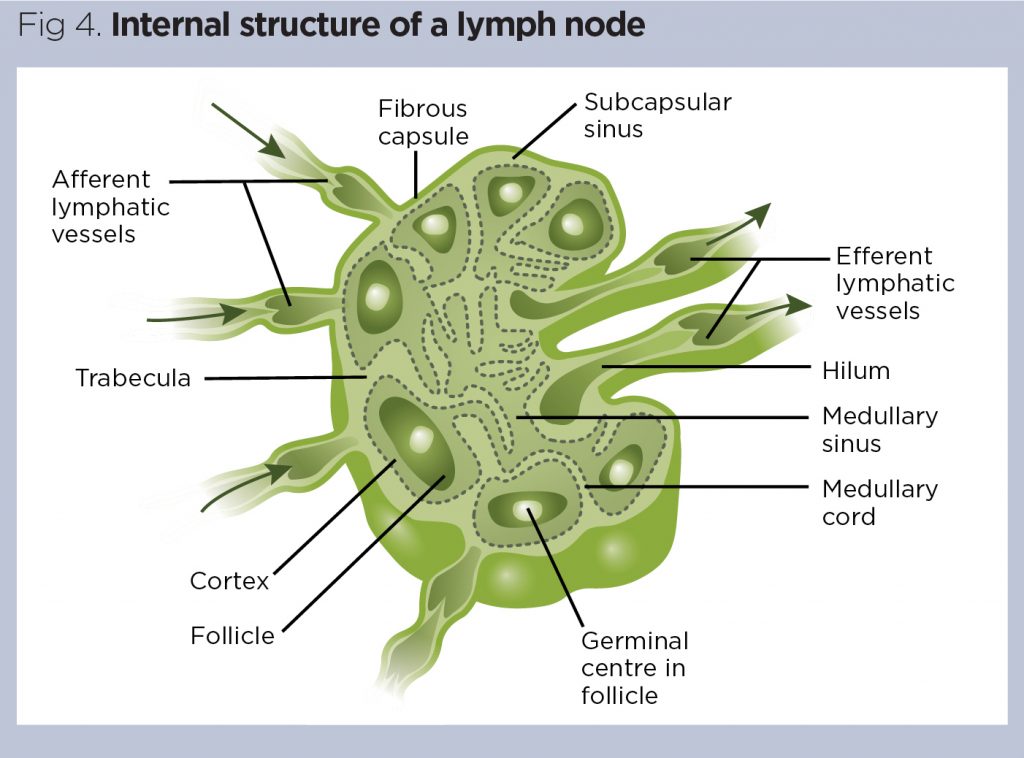
centrální části lymfatických uzlin jsou nezbytné pro jeho funkci; zde, tam jsou velké množství fixní makrofágy, které fagocytovat cizorodý materiál, např. bakterie při kontaktu a populací B – a T-buněk. Lymfatické uzliny jsou klíčové pro většinu protilátkami zprostředkované imunitní reakce: když fagocytární makrofágů past patogenní materiálu, že materiál je předkládán na lymfocyty, tak protilátky mohou být generovány.,
každá lymfatická uzlina je zásobována jednou nebo více aferentními lymfatickými cévami, které dodávají surovou nemodifikovanou lymfu přímo ze sousedních tkání. Zdravý, plně funkční uzel odstraňuje většinu patogenů z lymfy předtím, než tekutina opustí jednu nebo více eferentních lymfatických cév. Kromě lymfatického zásobování je každá lymfatická uzlina zásobována krví malou tepnou; tepna dodává různé leukocyty, které obývají vnitřní oblasti uzlu.,
když je přítomna infekce, lymfatické uzliny se stávají stále metabolicky aktivnějšími a jejich požadavky na kyslík se zvyšují. Malá žíla nese deoxygenovanou krev od každého uzlu a vrací ji do hlavních žil. V době infekce může tato žilní krev nést různé chemické posly (cytokiny), které produkují rezidentní leukocyty v uzlech. Tyto cytokiny působí jako obecné varovné signály, upozorňují tělo na potenciální hrozbu a aktivují řadu specifických imunitních reakcí.,
struktura
struktura lymfatické uzliny není na rozdíl od struktury sleziny. Každý lymfatických uzlin je rozdělen do několika oblastí:
- Vláknité kapsle – vytváří ochranný vnější plášť a má trabekuly, které rozšiřují pravidelně do uzlu, rozdělením do malých prostorů;
- Vnější kůry (nodulární cortex) – jen uvnitř kapsulární rozpětí, to se skládá z mnoha folikulů, které jsou bohaté na B-buňky., Když patogeny jsou přítomny, tyto folikuly rozšířit odhalit prominentní zárodečnými centry obsahujícími aktivně dělení, protilátky secernujících B-buněk;
- Vnitřní kůra (paracortex) – je to jen pod vnější kůry a je obzvláště bohatý na T-buňky, které také neustále obíhat po většině ostatních regionů uzlu;
- Prodloužená – centrální vnitřní část uzlu, který obsahuje velké množství pevných fagocytární makrofágů., Ty neustále monitorují lymfu pro potenciálně patogenní cizí materiál (proces známý jako immuno-dohled), který fagocytují při kontaktu.
Klinický význam
Během infekce, protilátky produkují B-buňky začnou množit v zárodečných center, což způsobuje postižené lymfatické uzliny zvětšit a stát hmatatelná a řízení. Některé z uvolněných cytokinů jsou pyrogenní (což znamená, že způsobují horečku) a působí přímo na termoregulační centrum v hypotalamu, aby se zvýšila tělesná teplota., Jako většina lidských patogenů rozdělit optimálně kolem 37°C, toto zvýšení tělesné teploty slouží k zpomalit bakteriální replikace, umožňující infekce, které mají být řešeny efektivněji imunitní systém. Otoky lymfatických uzlin a horečka jsou oba jisti, znamení, že tělo je montáž efektivní imunitní odpovědi proti obtěžování patogen; to se bude diskutovat podrobněji v části 3 této série.
existují i jiné lymfatické složky
jiné typy lymfatické tkáně., Slizniční lymfoidní tkáň (slad) je umístěna tak, aby chránila dýchací a gastrointestinální trakt před invazí mikrobů. Tyto jsou vyrobeny ze SLADU:
- Gut-associated lymphoid tissue;
- Bronchus-associated lymphoid tissue;
- palatine, kulturní a hltanu mandlí.
mandle jsou agregáty lymfatické tkáně strategicky umístěné, aby se zabránilo vniknutí cizího materiálu a patogenů do těla., Palatine mandle jsou v hltanu, lingvální mandle v dutině ústní a faryngální mandle (nosní mandle) jsou v zadní části nosní dutiny; v důsledku toho, mandle samy o sobě jsou na vysoké riziko infekce a zánětu (zánět mandlí). To bude také dále projednáno v části 3.,>Krevní a imunitní buňky jsou produkovány v červené kostní dřeně, během procesu se říká hematopoézou

- Otestujte si své znalosti s Pečovatelskou Krát sebehodnocení po přečtení tohoto článku., Pokud získáte skóre 80% nebo více, obdržíte osobní certifikát, který si můžete stáhnout a uložit do svého portfolia NT jako důkaz CPD nebo revalidace.
- Vezměte si Ošetřovatelství Krát Vlastní hodnocení pro tohoto článku.
Armstrong RA et al (2019) Úspěšné non-operativní řízení hemodynamicky nestabilní sleziny traumatická zranění: 4-leté případě série v BRITÁNII velké trauma centrum. European Journal of Trauma and Emergency Surgery; 45: 5, 933-938.,
Arnott a et al (2018) registr pro pacienty s asplenií/hyposplenismem snižuje riziko infekcí zapouzdřenými organismy. Klinické Infekční Nemoci; 67: 4, 557-561.
Baković D et al (2005) účinek kontrakce lidské sleziny na změnu počtu cirkulujících krvinek. Klinická a experimentální farmakologie a fyziologie; 32: 11, 944-951.
Bilder G (2016) lidský biologický Aggin: od makromolekul po orgánové systémy. Wiley.
Garnitschnig L et al (2020) postprandiální dynamika objemu sleziny u zdravých dobrovolníků. Fyziologické zprávy; 8: 2, e14319.,
Gujar s et al (2017) kadaverická studie lidské sleziny a její klinický význam. National Journal of Clinical Anatomy; 6: 1, 35-41.
małkiewicz A, Dziedzic M (2012) rekonverze kostní dřeně: zobrazování fyziologických změn v kostní dřeni. Polský žurnál radiologie; 77: 4, 45-50.
Pivkin IV et al (2016) biomechanika červených krvinek v lidské slezině a důsledky pro fyziologii a nemoci. Sborník Národní akademie věd Spojených států amerických; 113: 28, 7804-7809.,
Severa m et al (2019) Thymosiny u roztroušené sklerózy a její experimentální modely: přechod od základní k klinické aplikaci. Roztroušená skleróza a související poruchy; 27: 52-60.
Sherer y et al (1999) duální vztah mezi thymektomií a autoimunitou: kaleidoskop autoimunitního onemocnění. V: Paul s (ed) autoimunitní reakce. Současná Imunologie. Totowa, NJ: Humana Press.
Stewart IB, McKenzie DC (2002) lidská slezina během fyziologického stresu. Sportovní Medicína; 32: 6, 361-369.