US Pharm. 2010;35(8): HS2-HS4.
Staphylococcus aureus rezistentní na meticilin (MRSA) je jednou z hlavních příčin infekcí získaných ve zdravotnictví i v komunitě.1,2 infekce způsobené MRSA jsou spojeny s vysokým rizikem morbidity a úmrtnosti a vedou k vysokým nákladům na zdravotní péči.3-5 výskyt infekcí MRSA ve Spojených Státech stále rostl za posledních několik let z 22% v roce 1995 na 60% v roce 2003.,6 Health care–associated MRSA (HA-MRSA) je ve spojení s nemocnicích a zařízeních dlouhodobé péče a je běžné u pacientů s dlouhotrvající hospitalizace, minulosti antimikrobiální použití, dekubity, dialýza, permanentní katetry, enterální krmení, nebo historie IV zneužívání drog.7,8 v posledních letech však došlo k nárůstu nového kmene MRSA nazývaného MRSA související s komunitou (CA-MRSA)., To se zdá být získány v ambulantně, a přenos je prostřednictvím úzké fyzického kontaktu, jako v centrech denní péče, Indiánské rezervace, a nápravných zařízeních a u sportovců, vojenský personál, a muži, kteří mají sex s muži.7,9,10
Odlišení MRSA Kmenů
Několik zpráv odhalily rozdíly mezi HA-MRSA a CA-MRSA kmenů, včetně přítomnosti různých genotypů mezi dvěma kmeny. CA-MRSA je náchylná k několika beta-laktamovým antibiotikům, zatímco kmeny HA-MRSA nejsou., Kmeny CA-MRSA častěji kódují určité virulentní faktory, které byly spojeny s těžkou pneumonií (zejména u dětí) a infekcemi kůže a měkkých tkání u dospělých.8,11,12 CDC stanovila kritéria pro odlišení CA-MRSA od HA-MRSA. Tyto pokyny zahrnují izolaci pozitivní kultury MRSA do 48 hodin od přijetí pacienta do nemocnice. Být považován za CA-MRSA, pacient nesmí mít některý z následujících: poslední hospitalizace, přijetí do domu s pečovatelskou službou, hospic, nebo kvalifikované ošetřovatelské zařízení; dialýza; nebo nedávné operaci., Pacient také nesmí mít žádné indwelling katétry nebo jiné zdravotnické prostředky.13
Léčbě CA-MRSA
CDC doporučuje, aby řízení a prevence výskytu CA-MRSA patří zahrnující infekce, které produkují hnis, mytí rukou často, ne sdílení osobní položky, mytí znečištěné prádlo a oblečení s teplou vodou a sušení tkaniny v horkém sušičky oproti sušení na vzduchu.13 pro kožní abscesy zahrnuje léčba incizi a drenáž abscesů se systémovými antibiotiky nebo bez nich v závislosti na závažnosti infekce.,14
léčba CA-MRSA obvykle zahrnuje použití látek, jako je clindamycin, tetracykliny a trimethoprim-sulfamethoxazol (TMP-SMX). Antibiotikum rifampin by nikdy nemělo být používáno jako monoterapie pro léčbu MRSA. Rezistence se rychle rozvíjí s monoterapií rifampinem; při použití v kombinaci s jiným činidlem proti MRSA však může účinněji vymýtit organismy z nosných míst.15 výše uvedená antibiotika jsou obvykle životaschopné možnosti léčby u pacientů léčených ambulantně., V závažných infekcí, které vyžadují hospitalizaci, NITROŽILNÍ antibiotika včetně vankomycin, linezolid, quinupristin-dalfopristin, daptomycin, tigecyklin, a telavancin jsou vhodné terapie, které mohou být použity (TABULKA 1).
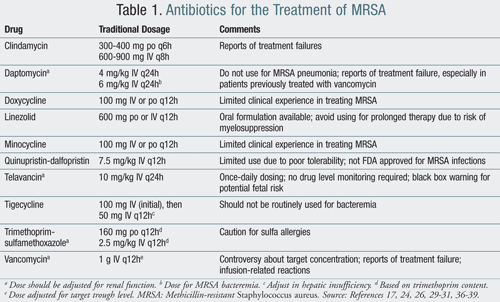
i když klindamycin (Cleocin) by mohly být použity pro CA-MRSA, byla zaznamenána rezistence až na 19% u pacientů léčených přípravkem. Pacienti léčeni klindamycinem proto musí být bedlivěji sledováni, aby se vyvinula vlastní indukovaná rezistence.,16 Clindamycin byl také spojen s vývojem infekcí Clostridium difficile, což omezilo jeho použití po delší dobu.17
TMP-SMX (Bactrim) může být v některých případech MRSA infekcí považován za alternativu k léčbě vankomycinem. Stejně jako u klindamycinu však existují zprávy o selhání léčby. Tato terapie má také omezené použití kvůli vysokému výskytu sulfonamidových alergií, které se vyskytly až u 10% populace.,18
minocyklin (Minocin) a doxycyklin (Vibramycin) jsou tetracyklinová antibiotika, která byla použita k léčbě MRSA. Tyto látky mají pouze omezené údaje o použití v MRSA, ale klinický úspěch byl hlášen.19
léčba HA-MRSA
parenterální antibiotika jsou považována za zlatý standard pro léčbu HA-MRSA. Po několik desetiletí se široce používá glykopeptidové antibiotikum vankomycin.
vankomycin (Vancocin) inhibuje syntézu buněčné stěny; má však pomalejší baktericidní aktivitu in vitro., S jeho nadužíváním se objevily zprávy o snížené náchylnosti a výskytu vancomycinové heteroresistence u s aureus.20,21 nárůst subpopulace S. aureus, s minimální inhibiční koncentrací (MIC) >2 mcg/mL vankomycinu (dále MIC tečení) je spojena s oběma microbiologic a klinické selhání. Národní výbor pro klinické laboratorní standardy (NCCLS) navrhl nové body přerušení pro vankomycin—změna MIC pro „citlivé“ z ≤4 mcg/mL na ≤2 mcg/ml.,22 zdůvodnění tohoto návrhu je částečně založeno na neoficiálních klinických pozorováních selhání léčby během léčby standardními dávkami vankomycinu u pacientů s MIC 4 mcg / ml. Kromě toho mohou být u závažných infekcí, jako je pneumonie a osteomyelitida, vyžadovány vyšší minimální hladiny (tj. minimální hladiny 15-20 mcg/mL) v důsledku špatné penetrace tkáně vankomycinem. Tam byly některé neoficiální zprávy o možné nefrotoxicity spojené s těmito vysokými minimálními hladinami.,
Jeffres et al představil abstraktní v roce 2006 Interscience Conference on Antimicrobial Agents and Chemotherapy (ICAAC), který zhodnotil riziko nefrotoxicity s vyšší minimální hladiny vankomycinu.23 Ve své studii se uvádí 30% riziko nefrotoxicity (definována jako zvýšení o 0,5 mg/dL nebo 50% zvýšení sérového kreatininu před zahájením léčby) u pacientů s vankomycin minimální hladiny 315 ug/mL, ve srovnání s 13% u pacientů s minimální hladiny <15 mcg/mL.23 některé populace pacientů jsou vystaveny vyššímu riziku vývoje nefrotoxicity vyvolané vankomycinem., Patří mezi ně známé rizikové faktory, jako je starší věk, kriticky nemocné, s nižší funkcí ledvin a současné užívání jiných nefrotoxických látek, jako jsou aminoglykosidy. Všechny tyto faktory vedly ke zvýšení potřeby a použití novějších agentů.
Linezolid (Zyvox) je první oxazolidinone schválen pro léčbu infekcí kůže a měkkých tkání, bakteriémie, a komunitní a nozokomiální pneumonie způsobené MRSA.24 inhibuje zahájení syntézy proteinů v ribozomu 50. let; na rozdíl od většiny ostatních léků je to bakteriostatické činidlo., Výhody jeho použití patří dostupnost ústní formulaci, že má vynikající biologické vlastnosti, se žádná úprava dávky je zapotřebí u pacientů s renální insuficiencí, včetně pacientů užívajících renální substituční terapie. Jedním limitujícím faktorem pro jeho použití, zejména pro delší dobu trvání léčby, je myelosuprese u pacientů, kteří dostávali linezolid déle než 14 dní.24,25 ačkoli je k dispozici jako perorální formulace, nepoužívá se tolik v ambulantním prostředí kvůli jeho nákladům., To také není pokryto v mnoha pojistných smlouvách, takže pacienti mohou potřebovat používat programy pomoci pacientům výrobce.
Daptomycin (Cubicin), lipopeptide antibiotika s rychlým baktericidním činnosti, je schválen pro léčbu komplikovaných infekcí kůže a měkkých tkání, stejně jako bakteriémie způsobené MRSA.26 jeho mechanismus účinku zahrnuje depolarizaci bakteriální buněčné stěny. Nežádoucí účinky daptomycinu zahrnují zvýšenou kreatinkinázu (CK) a rabdomyolýzu, zejména u pacientů užívajících souběžné inhibitory HMG-CoA reduktázy (statiny)., Proto musí být týdenní hladiny CK čerpány, zatímco pacient dostává daptomycin. Je třeba také poznamenat, že byly hlášeny případy rezistence MRSA na daptomycin, zejména při dlouhodobém užívání a u pacientů s předchozí expozicí vankomycinu.26-28 Daptomycin by neměl být používán k léčbě MRSA pneumonie, protože jeho aktivita je inhibována plicními povrchově aktivními látkami.
Quinupristin-dalfopristin (Synercid) je streptogramin, který má aktivitu proti MRSA., Přestože FDA není schválena pro použití u infekcí MRSA, používá se u infekcí kůže a měkkých tkání u pacientů, kteří netolerují léčbu vankomycinem nebo selhávají. Vzhledem k tomu, že tato léčba byla pacientům špatně tolerována, je její použití v klinické praxi omezené.29 mezi hlavní nežádoucí účinky patří hyperbilirubinémie, myalgie a artralgie. Na základě těchto faktorů se tento přípravek používá pouze jako poslední možnost, když pacienti selhali nebo nemohou tolerovat jiné látky.,
novější terapie
Tigecyklin (Tygacil) je prvním bakteriostatickým činidlem ve třídě antibiotik glycylcyklinu (syntetický derivát tetracyklinu). Je indikován k léčbě komplikovaných infekcí kůže a struktury kůže (cSSSI), komplikovaných intraabdominálních infekcí a komunitní pneumonie způsobené MRSA.30 Tigecyklin by neměl být běžně používán pro bakterémii kvůli obavám z dosažení nedostatečných hladin v séru., Protože tigecyklin je široký-antibiotikum spektra, jeho použití by mělo být omezeno na závažné a život ohrožující infekce u hospitalizovaných pacientů.
Telavancin (Vibativ) je nejnovější lék, který má být schválen FDA pro léčbu infekcí MRSA.31 jedná se o lipoglykopeptid podobný vankomycinu, i když se jeho mechanismus účinku liší. Telavancin narušuje propustnost buněčné membrány tím, že depolarizace plazmatické membrány, zvýšení permeability a úniku buněčného adenosintrifosfátu a draslíku (K+)., Načasování těchto změn koreluje s rapidní, na koncentraci závislou ztrátu bakteriální životaschopnost, což naznačuje, že brzy baktericidní aktivitu telavancin výsledky z odvodu z buňky, membránový potenciál a zvýšení permeability membrány.
klinické studie ukázaly, že telavancin není při léčbě cSSSI nižší než vankomycin.32,33 jednou z výhod telavancinu nad vankomycinem je dávkování jednou denně a není třeba sledovat hladiny léků. Stejně jako vankomycin je však třeba dávku upravit u pacientů s renální insuficiencí.,31 funkce ledvin musí být sledována během a po ukončení léčby u všech pacientů. Telavancin je spojen s prodloužením QTc a musí být používán s opatrností u pacientů s léky, které by mohly také prodloužit QTc. V klinických studiích porovnávajících telavancin s vankomycin, nežádoucí účinky hlášené u více než 10% pacientů léčených s telavancin zahrnuty poruchy chuti, nevolnost, zvracení, a pěnivý moči.31 závažných nežádoucích účinků bylo hlášeno u 7% pacientů léčených telavancinem a nejčastěji zahrnovalo renální, respirační nebo srdeční příhody., Existuje upozornění na černou skříňku týkající se rizika plodu spojeného s užíváním telavancinu; ženy v plodném věku tedy musí mít před zahájením telavancinu sérový těhotenský test.31
ceftobiprol (Zeftera) je první cefalosporin s baktericidní aktivitou proti MRSA. Jeho antibakteriální aktivita zahrnuje inhibici proteinů vázajících penicilin, které se podílejí na syntéze buněčné stěny. V klinických studiích byla stejně účinná jako kombinace vankomycinu a ceftazidimu při léčbě cSSSI.,34 je obecně dobře snášen, s hlavními nežádoucími účinky léku, včetně nevolnosti a poruch chuti. Ceftobiprole je není v současné době schválen pro použití v USA, a i když to byl dříve schválen pro použití v Kanadě, výrobce ukončena prodej drog od 16. dubna 2010.35 To bylo následující doporučení od regulačních orgánů v Evropě (Evropský Výbor pro Léčivé Přípravky pro Humánní Použití) a USA (FDA) schválil lék., I když fáze III výsledky naznačily přínos ceftobiprole, tam byly obavy, pokud jde o integritu těchto výsledků studie v důsledku manipulace s klinickými daty z některé ze studijních míst. S tímto nedávným vývojem zůstává budoucnost použití ceftobiprolu na americkém trhu sporná.
Závěr
S příchodem CA-MRSA, stejně jako hetero-rezistentní MRSA, je důležité, aby lékárníci být obeznámeni s všechny prostředky k dispozici pro řízení infekcí MRSA. Je také nezbytné zvolit vhodné antimikrobiální činidlo pro léčenou infekci., Kromě toho by činidla se širším spektrem aktivity (např. tigecyklin) měla být vyhrazena pro velmi závažné infekce a při stanovení multipatogenních infekcí. Je také nanejvýš důležité rezervovat novější látky pro závažnější infekce, aby se minimalizoval vývoj rezistence.
1. Boucher HW, Corey GR. Epidemiologie Staphylococcus aureus rezistentní na meticilin. Clin Infikovat Dis.
2. Styers D, Sheehan DJ, Hogan P, et al., Laboratorní sledování současných vzorců antimikrobiální rezistence a trendů mezi Staphylococcus aureus: stav 2005 ve Spojených státech. Ann Clin Microbiol Antimikrob. 2006;5:2.
3. Chien JW, Kucia ML, Salata RA. Použití linezolidu, oxazolidinonu, při léčbě grampozitivních bakteriálních infekcí rezistentních na více léčiv. Clin Infikovat Dis. 2000;30:146-151.
4. Soriano A, Martinez JA, Mensa J, et al. Patogenní význam rezistence na meticilin u pacientů s bakteremií Staphylococcus aureus. Clin Infikovat Dis. 2000;30:368-673.
5. Graffunder EM, Venezia RA., Rizikové faktory spojené s infekcí rezistentní na nozokomiální meticilin Staphylococcus aureus (MRSA) včetně předchozího použití antimikrobiálních látek. J Antimikrob Chemother. 2002;49:999-1005.
6. Klevens RM, Edwards JR, TENOVER FC, et al. Změny v epidemiologii Staphylococcus aureus rezistentní na meticilin v jednotkách intenzivní péče v amerických nemocnicích, 1992-2003. Clin Infikovat Dis.
7. Levine DP, Cushing RD, Jui J, Brown WJ. Komunitní meticilin rezistentní Staphylococcus aureus endokarditida v Detroit Medical Center. Ann Stážistka Med. 1982;97:330-338.
8., Lodise TP Jr, McKinnon PS, Rybak m. Predikční model pro identifikaci pacientů s bakterií Staphylococcus aureus s rizikem rezistence na meticilin. Infikovat Kontrolní Hosp Epidemiol. 2003;24:655-661.
9. Král MD, Humphrey BJ, Wang YF, et al. Vznik komunitně získaného klonu Staphylococcus aureus USA 300 rezistentního na meticilin jako převládající příčina infekcí kůže a měkkých tkání. Ann Stážistka Med. 2006;144:309-317.
10. Centra pro kontrolu a prevenci nemocí., Infekce Staphylococcus aureus rezistentní na meticilin mezi konkurenčními účastníky sportu-Colorado, Indiana, Pennsylvania a Los Angeles County, 2000-2003. MMWR. 2003;52:793-795.
11. Lowy FD. Infekce Staphylococcus aureus. N Engl J Med. 1998;339:520-532.
12. Chambers HF. Měnící se epidemiologie Staphylococcus aureus? Vynořit Infikovat Dis.
13. Informace o MRSA související s komunitou pro lékaře. NEMOCNOST. www.cdc.gov/ncidod/dhqp/ar_ 2008; 46 (suppl 5): s344-s349. 2006;42:389-391. 2001;7:178-182.mrsa_ca_clinicians.html. Přístupné 4. Července 2010.
14. Rybak MJ, LaPlante kl., Staphylococcus aureus spojený s meticilinem; přezkum. Farmakoterapie. 2005;25:74-85.
15. Gorwitz RJ, Jernigan DB, Powers JH, et al. Strategie klinického řízení MRSA ve Společenství: shrnutí setkání odborníků svolaného centry pro kontrolu a prevenci nemocí. Března 2006. www.cdc.gov/ncidod/dhqp/pdf/ar/CAMRSA_ExpMtgStrategies.pdf. přístup k 4. červenci 2010.
16. Sabol KE, Echevarria KL, Lewis JS II. Staphylococcus aureus rezistentní na meticilin: nová chyba, staré drogy. Ann Pharmacother. 2006;40:1125-1133.
17., Cleocin (clindamycin) příbalová informace. New York, NY: Pfizer Inc; listopad 2005.
18. Strom BL, Schinnar R, Apter AJ, et al. Absence zkřížené citlivosti mezi sulfonamidovými antibiotiky a sulfonamidovými nonantibiotiky. N Engl J Med. 2003;349:1628-1635.
19. Nicolau DP, Freeman CD, Nightingale CH, et al. Minocyklin versus vankomycin pro léčbu experimentální endokarditidy způsobené Staphylococcus aureus rezistentním na oxacilin. Antimikrobní Látky Chemother. 1994;38:1515-1518.
20. Sakoulas G, Moellering RC Jr., Zvýšení antibiotické rezistence u kmenů Staphylococcus aureus rezistentních na meticilin. Clin Infikovat Dis. 2008; 46 (suppl 5):S360-S367.
21. Rybak MJ, Akins RL. Vznik meticilin-rezistentní Staphylococcus aureus s intermediární glykopeptidy rezistence: klinický význam a možnosti léčby. Droga. 201;61:1-7.
22. Tenover FC, Moellering RC Jr. důvody pro revizi Clinical and Laboratory Standards Institute vankomycin minimální inhibiční koncentrace interpretační kritéria pro Staphylococcus aureus. Clin Infikovat Dis. 2007;44:1208-1215.
23., Jeffres MN, Micek ST, Isakow W, et al. Zvýšený výskyt nefrotoxicity s vyššími koncentracemi vankomycinu v séru. Program a abstrakty 46. konference Interscience o antimikrobiálních látkách a chemoterapii( ICAAC); září 27-30, 2006; San Francisco, CA. Abstrakt K789.
24. Zyvox (linezolid) příbalová informace. New York, NY: Pfizer Inc; prosinec 2009.
25. Kuter DJ, Tillotson GS. Hematologické účinky antimikrobiálních látek, zaměření na oxazolidinon, linezolid. Farmakoterapie. 201;21:1010-1013.
26. Cubicin (daptomycin) příbalová informace., Lexington, MA: Cubist Pharmaceuticals; January 2010.
27. Murthy MH, Olson ME, Wickert RW, et al. Daptomycin non-susceptible methicillin-resistant Staphylococcus aureus USA 300 isolate. J Med Microbiol. 2008;57:1036-1038.
28. Mangili A, Bica I, Snydman R, Hamer DH. Daptomycin-resistant methicillin-resistant Staphylococcus aureus bacteremia. Clin Infect Dis. 2005;40:1058-1060.
29. Synercid (quinupristin-dalfopristin) package insert. Greenville, NC: Monarch Pharmaceuticals; June 2008.
30. Tygacil (tigecycline) package insert. Philadelphia, PA: Wyeth Pharmaceuticals; September 2009.,
31. Vibativ (telavancin) příbalová informace. Deerfield, IL: Astellas Pharma US, Inc; září 2009.
32. Stryjewski ME, Chu VH, O ‚ Riordan WD, et al. Telavancin versus standardní terapie pro léčbu komplikovaných infekcí kůže a struktury kůže způsobených gram pozitivními bakteriemi: FAST 2 studie. Antimikrobní Látky Chemother. 2006;50:862-867.
33. Corey GR. Studie telavancinu v cSSSI. Příspěvek prezentovaný na: třetím mezinárodním sympoziu o rezistentních grampozitivních infekcích; 10. října 2006; Niagara-on-the-Lake, Kanada.
34. Vidaillac C, Rybak MJ., Ceftobiprole: first cephalosporin with activity against methicillin-resistant Staphylococcus aureus. Pharmacotherapy. 2009;29:511-525.
35. Discontinuation of the sale of ceftobiprole in Canada. Basilea Pharmaceutica. April 9, 2010. http://hugin.info/134390/R/1401931/356785.pdf. Accessed July 12, 2010.
36. Vibramycin (doxycycline) package insert. New York, NY: Pfizer Inc; April 2007.
37. Minocin (minocycline) package insert. Philadelphia, PA: Triax Pharmaceuticals; March 2006.
38. Bactrim (trimethoprim-sulfamethoxazole) package insert. Philadelphia, PA: AR Scientific; November 2006.
39., Vancocin (vancomycin) package insert. Exton, PA: ViroPharma Inc; October 2005.