Srážky Reakce a Rozpustnost Pravidla
srážecí reakce je taková, ve které rozpuštěné látky reagují za vzniku jednoho (nebo více) pevných produktů. Mnoho reakcí tohoto typu zahrnují výměnu iontů mezi iontové sloučeniny ve vodném roztoku a jsou někdy označovány jako dvojí výchylky, dvakrát výměna, nebo metathesis reakce., Tyto reakce jsou běžné v přírodě a jsou zodpovědné za tvorbu korálových útesů ve vodách oceánu a ledvinových kamenů u zvířat. Jsou široce používány v průmyslu pro výrobu řady komoditních a speciálních chemikálií. Srážení reakce rovněž hrát ústřední roli v mnoha chemických metod analýzy, včetně namátkových testů používaných k identifikaci kovových iontů a gravimetrické metody pro stanovení složení hmoty (viz poslední modul v této kapitole).,
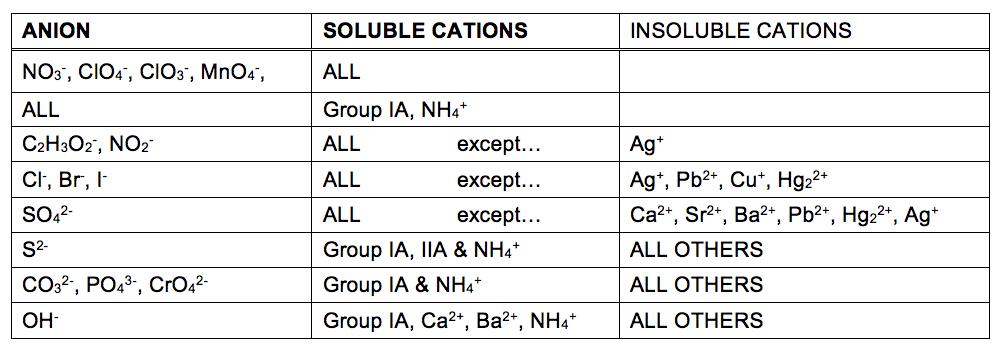
rozsah, v jakém může být látka rozpuštěna ve vodě nebo v jakémkoli rozpouštědle, je kvantitativně vyjádřen jako její rozpustnost, definovaná jako maximální koncentrace látky, které lze za stanovených podmínek dosáhnout. Látky s relativně velkými rozpustnostmi jsou považovány za rozpustné. Látka se vysráží, když jsou podmínky roztoku takové, že její koncentrace překračuje rozpustnost. Látky s relativně nízkou rozpustností se říká, že jsou nerozpustné, a to jsou látky, které snadno vysrážení z roztoku., Více informací o těchto důležitých pojmech naleznete v textové kapitole o řešeních. Pro účely předpovídání identit pevných látek vytvořených srážecími reakcemi lze jednoduše odkazovat na vzorce rozpustnosti, které byly pozorovány u mnoha iontových sloučenin (Tabulka 1).
názorným příkladem srážek je pozorován při řešení jodidu draselného a vést dusičnanů jsou smíšené, což vede k tvorbě pevných vést jodid:
Toto pozorování je v souladu s rozpustností pokyny: pouze nerozpustné sloučeniny mezi všechny zúčastněné je vést jodid, jedna z výjimek z obecné rozpustnost jodidu soli.,
čisté iontové rovnice představuje tato reakce je:
Vést jodid je jasně žlutá pevná látka, která byla dříve využívána jako umělecký pigment známý jako jód žlutá (Obrázek 1). Vlastnosti čistých krystalů PbI2 je činí užitečnými pro výrobu rentgenových a gama detektorů.

rozpustnost tabulky v Tabulce 1 mohou být použity ke stanovení, zda srážecí reakce se vyskytují při řešení rozpustné iontové sloučeniny jsou smíchány dohromady. Člověk potřebuje pouze identifikovat všechny ionty přítomné v roztoku a pak zvážit, zda je to možné kationtové/aniontové párování by mohlo mít za následek nerozpustnou sloučeninu.
například míchání roztoků dusičnanu stříbrného a fluoridu sodného přinese roztok obsahující AG+, NO3−, na+ A F− ionty., Kromě dvou iontových sloučenin původně přítomných v roztocích, AgNO3 a NaF, mohou být z této sbírky iontů odvozeny dvě další iontové sloučeniny: NaNO3 a AgF.
tabulka rozpustnosti uvádí, že všechny dusičnanové soli jsou rozpustné, ale že AgF je jednou z výjimek z obecné rozpustnosti fluoridových solí. Předpokládá se tedy srážková reakce, jak je popsáno v následujících rovnicích: