Niederschlagsreaktionen und Löslichkeitsregeln
Eine Niederschlagsreaktion ist eine, bei der gelöste Substanzen unter Bildung eines (oder mehrerer) fester Produkte reagieren. Viele Reaktionen dieser Art beinhalten den Austausch von Ionen zwischen ionischen Verbindungen in wässriger Lösung und werden manchmal als Doppelverschiebung, Doppelersatz oder Metathesereaktionen bezeichnet., Diese Reaktionen sind häufig in der Natur und sind verantwortlich für die Bildung von Korallenriffen in Meerwasser und Nierensteine bei Tieren. Sie werden in der Industrie für die Produktion einer Reihe von Waren-und Spezialchemikalien weit verbreitet. Niederschlagsreaktionen spielen auch bei vielen chemischen Analysetechniken eine zentrale Rolle, einschließlich Punkttests zur Identifizierung von Metallionen und gravimetrischen Methoden zur Bestimmung der Zusammensetzung der Materie (siehe das letzte Modul dieses Kapitels).,
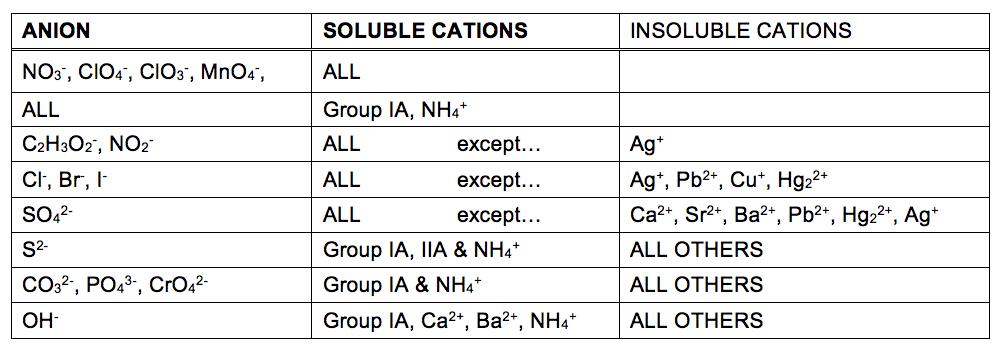
Das Ausmaß, in dem ein Stoff in Wasser oder einem Lösungsmittel gelöst werden kann, wird quantitativ als seine Löslichkeit ausgedrückt, definiert als die maximale Konzentration eines Stoffes, die unter bestimmten Bedingungen erreicht werden kann. Substanzen mit relativ großen Löslichkeiten sollen löslich sein. Eine Substanz fällt aus, wenn die Lösungsbedingungen so sind, dass ihre Konzentration ihre Löslichkeit übersteigt. Substanzen mit relativ geringen Löslichkeiten gelten als unlöslich, und dies sind die Substanzen, die leicht aus der Lösung ausfallen., Weitere Informationen zu diesen wichtigen Konzepten finden Sie im Textkapitel Lösungen. Um die Identitäten von Feststoffen vorherzusagen, die durch Niederschlagsreaktionen gebildet werden, kann man sich einfach auf Löslichkeitsmuster beziehen, die für viele ionische Verbindungen beobachtet wurden (Tabelle 1).
Ein anschauliches Beispiel für Niederschlag wird beobachtet, wenn Lösungen von Kaliumiodid und Bleinitrat gemischt werden, was zur Bildung von festem Bleiiodid führt:
Diese Beobachtung steht im Einklang mit den Löslichkeitsrichtlinien: Die einzige unlösliche Verbindung unter allen Beteiligten ist Bleiiodid, eine der Ausnahmen von der allgemeinen Löslichkeit von Iodidsalzen.,
Die net Ionische Gleichung für diese Reaktion lautet:
– Blei-Iodid ist ein hell gelber Feststoff, der früher als ein Künstler pigment, bekannt als JOD-gelb (Abbildung 1). Die Eigenschaften von reinen PbI2-Kristallen machen sie nützlich für die Herstellung von Röntgen-und Gammastrahlendetektoren.

Die Löslichkeitstabelle in Tabelle 1 kann verwendet werden, um vorherzusagen, ob eine Fällungsreaktion auftritt, wenn Lösungen löslicher ionischer Verbindungen miteinander vermischt werden. Man muss lediglich alle in der Lösung vorhandenen Ionen identifizieren und dann prüfen, ob eine Kation/Anion-Paarung zu einer unlöslichen Verbindung führen kann.
Zum Beispiel ergibt das Mischen von Lösungen von Silbernitrat und Natriumfluorid eine Lösung, die Ag+−, NO3−, Na+ – und F-Ionen enthält., Abgesehen von den beiden ursprünglich in den Lösungen AgNO3 und NaF vorhandenen ionischen Verbindungen können aus dieser Ionensammlung zwei zusätzliche ionische Verbindungen abgeleitet werden: NaNO3 und AgF.
Die Löslichkeitstabelle zeigt an, dass alle Nitratsalze löslich sind, dass AgF jedoch eine der Ausnahmen von der allgemeinen Löslichkeit von Fluoridsalzen ist. Es wird daher vorausgesagt, dass eine Niederschlagsreaktion auftritt, wie sie durch die folgenden Gleichungen beschrieben wird: